EUDAMED: Se publica el plan de implementación actualizado para 2025–2027
La Comisión Europea ha publicado un plan actualizado para el despliegue de EUDAMED, introduciendo cambios en el calendario de implementación y en los períodos transitorios.
Las empresas del sector MedTech deben prestar especial atención a estas actualizaciones para garantizar el cumplimiento de los requisitos de UDI y de vigilancia postcomercialización.
🔗 Fuente oficial: : EUDAMED Roadmap (European Commission)
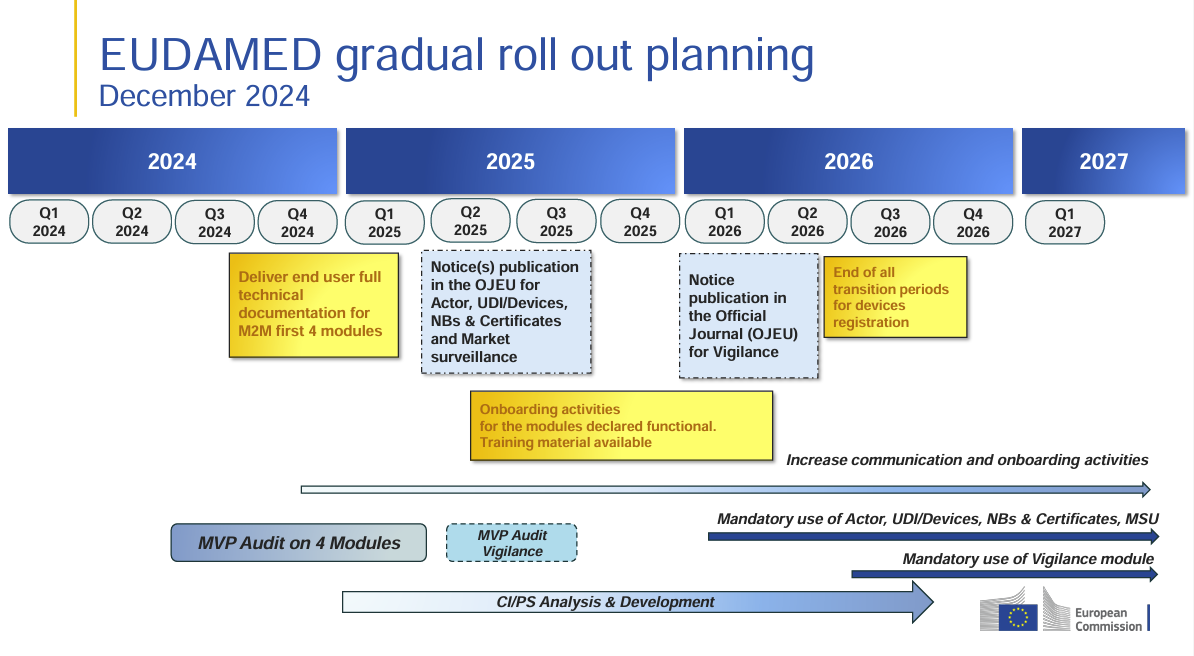
Cambios clave en el despliegue de EUDAMED (a diciembre de 2024)
🔹 4.º trimestre de 2024: Publicación de la documentación técnica completa para los módulos M2M
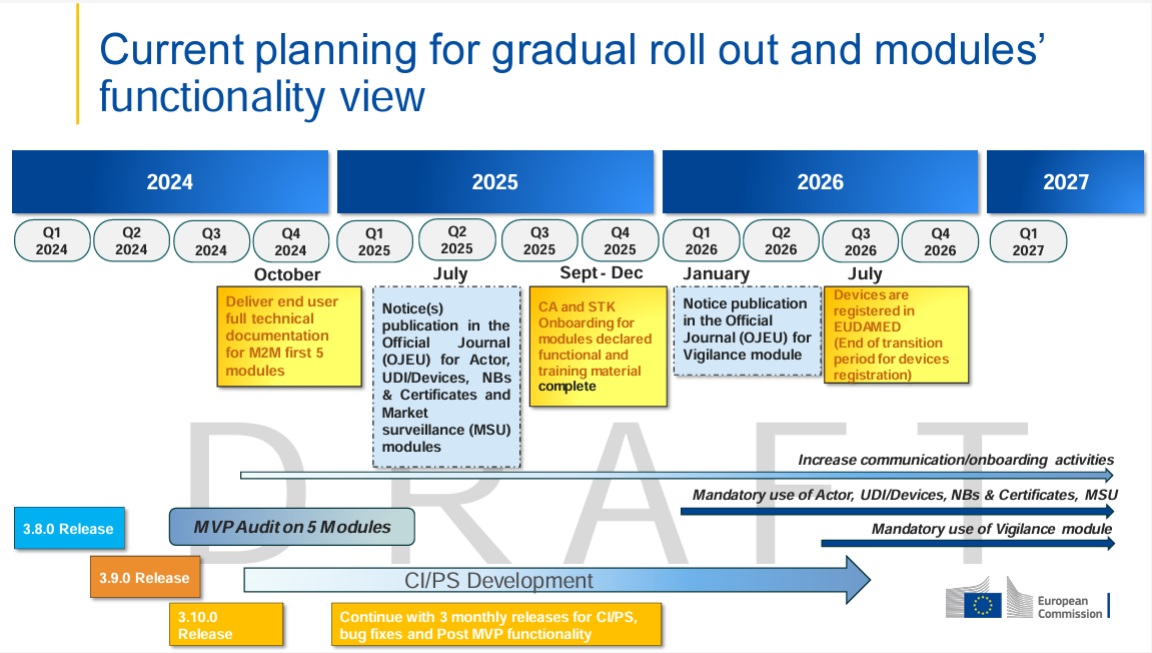
Versión de julio 2024: abarcaba 5 módulos
Versión de diciembre 2024: reducida a 4 módulos
🔹 2.º trimestre de 2025: Publicación en el Diario Oficial de la UE (DOUE) para los módulos clave
Sin cambios – sigue aplicando a: Actores, UDI/Dispositivos, Organismos Notificados y Certificados, y Vigilancia del Mercado (MSU)
🔹 3.º trimestre de 2025: Incorporación a los módulos funcionales
Versión de julio 2024: “Incorporación de CA y STK con materiales de formación completos”
Versión de diciembre 2024: Redacción más general: “Actividades de incorporación y materiales de formación disponibles”
🔹 1.º trimestre de 2026: Publicación del módulo de Vigilancia en el DOUE
Sin cambios
🔹 3.º trimestre de 2026: Fin del período de transición para el registro de dispositivos
Versión de julio 2024: “Los dispositivos se registran en EUDAMED (fin del período de transición para el registro de dispositivos)”
Versión de diciembre 2024: “Fin de todos los períodos de transición para el registro de dispositivos”
Mayor énfasis en la finalización definitiva de los plazos transitorios
¿Por qué es importante para las empresas MedTech?
🔸 Uso obligatorio de los módulos EUDAMED a partir de 2026 para UDI, Vigilancia, Vigilancia del mercado y Certificados
🔸 Período de preparación más corto para la integración M2M debido a la reducción del número inicial de módulos
🔸 Nuevas actividades de formación e incorporación para garantizar una transición fluida







Related Posts