Global Submission Portal: La nueva era del cumplimiento normativo

Plataforma unificada para registros globales ante la FDA y EUDAMED ya disponible
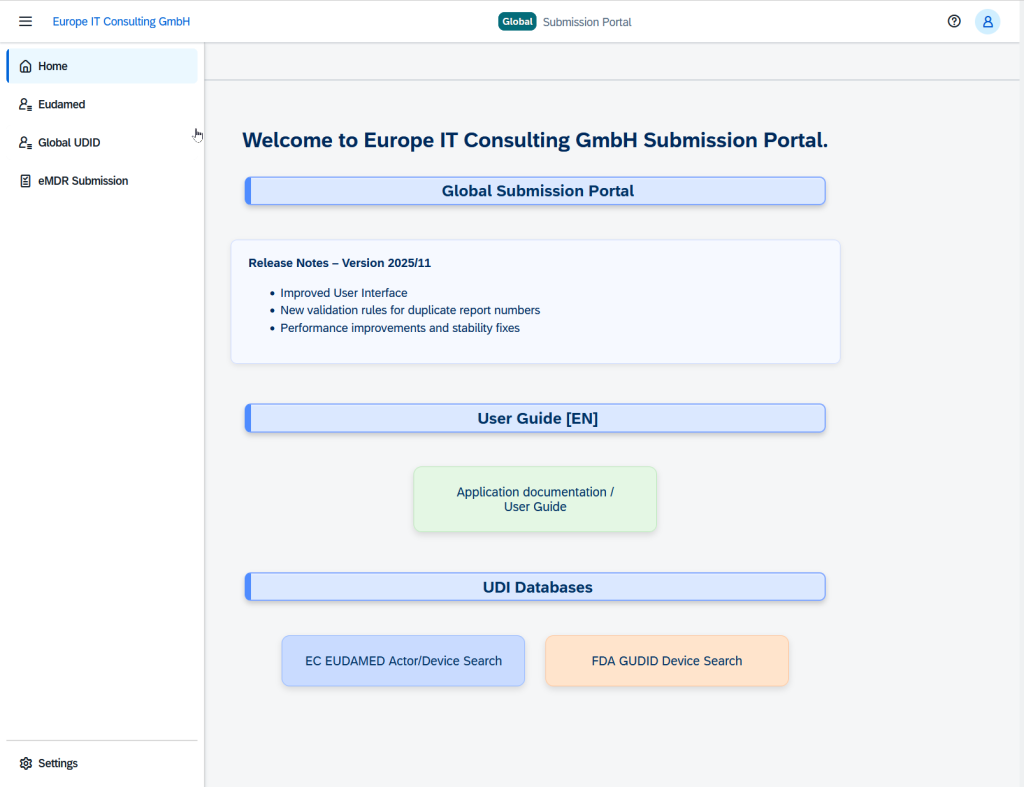
Europe IT Consulting se complace en anunciar el lanzamiento del Global Submission Portal – una solución revolucionaria diseñada para simplificar y acelerar los procesos de cumplimiento normativo para los fabricantes de dispositivos médicos en todo el mundo.
El Desafío
Los fabricantes de dispositivos médicos se enfrentan a la compleja tarea de registrar e informar sus productos ante diversas autoridades a nivel mundial. Cada autoridad tiene sus propios requisitos, formatos y procesos, lo que conlleva a:
- Procesos manuales que consumen mucho tiempo
- Alto riesgo de errores en la captura de datos
- Falta de transparencia sobre el estado de los registros
- Flujos de trabajo fragmentados en múltiples sistemas
La Solución: Global Submission Portal
Nuestro Global Submission Portal integra múltiples flujos de trabajo de registro en una única plataforma fácil de usar. Los fabricantes y los equipos de asuntos regulatorios pueden ahora enviar conjuntos de datos relevantes para el cumplimiento directamente a las autoridades de todo el mundo, de manera eficiente, segura y transparente.
Visite nuestra página de destino dedicada al GSP
¿Busca una solución diseñada específicamente para gestionar altos volúmenes de datos? En nuestra página de destino especializada, le mostramos cómo escalar y validar registros UDI complejos de forma eficiente.
Funcionalidad principal
El portal automatiza todo el proceso de envío: desde la recopilación de datos basada en Excel hasta la validación automática y la transmisión directa a las autoridades, todo en un flujo de trabajo continuo.
Módulos compatibles
Actualmente, el portal admite cuatro áreas críticas de cumplimiento:
- 🇺🇸 FDA eMDR: Informes electrónicos de dispositivos médicos para notificaciones rápidas a la FDA.
- 🇺🇸 FDA GUDID: Base de datos global de UDI para el registro en el mercado estadounidense.
- 🇪🇺 EUDAMED UDI: Envíos de UDI conformes con la MDR de la UE.
- 🇪🇺 EUDAMED Vigilance: Informes de incidentes de fabricantes para la UE.
Funciones clave en detalle
Carga basada en Excel y grandes volúmenes de datos
Simplemente cargue sus archivos Excel preparados. Nuestra solución está diseñada explícitamente para **altos volúmenes**, lo que permite procesar miles de registros en el menor tiempo posible. El sistema reconoce automáticamente la estructura de los datos y prepara el envío.
GUDI – El Add-on de SAP UDI para el cumplimiento global.
Plazos de cumplimiento: EUDAMED y swissdamed
Los requisitos regulatorios se están endureciendo: el uso obligatorio de EUDAMED para el registro de productos se acerca. En Suiza, la obligación de registro a través de swissdamed ya es obligatoria para muchos actores. Nuestro portal le ayuda a cumplir estos plazos de forma segura mediante procesos automatizados.
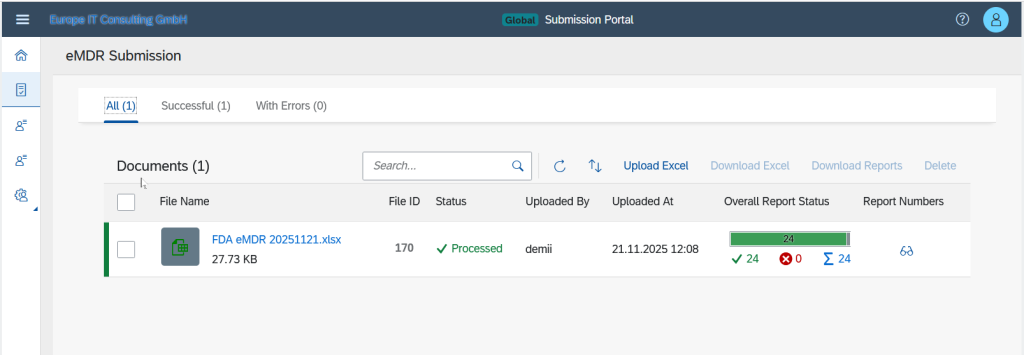
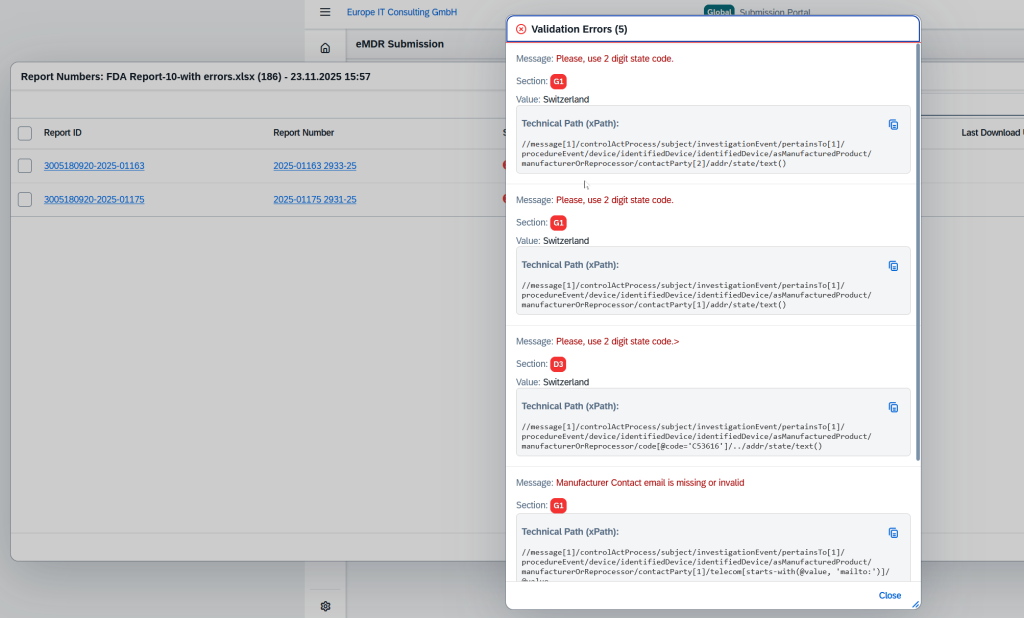
Errores de validación y estado en tiempo real
En caso de transmisiones fallidas, se muestran errores de validación detallados. Cada envío pasa por fases de estado transparentes: Uploaded (Cargado), Processing (Procesando), Success (Exitoso) o Failed (Fallido).
Seguridad y cumplimiento
- Transmisión de datos cifrada (TLS/SSL)
- Aislamiento estricto de datos por cliente
- Pista de auditoría para todas las actividades
Desarrollo continuo
El Global Submission Portal se actualiza continuamente para admitir nuevos requisitos regulatorios. Las expansiones planificadas incluyen autoridades internacionales adicionales y módulos de cumplimiento extra.
¿Nos vemos en la Regularia 2026?
Visítenos el 03 de marzo de 2026 en Tuttlingen. ¡Estaremos encantados de mostrarle nuestras soluciones GSP y SAP en vivo!
Conclusión
Con el Global Submission Portal, Europe IT Consulting ofrece una solución moderna y eficiente para los desafíos del cumplimiento normativo global. ¡Experimente usted mismo cómo el portal revoluciona sus flujos de trabajo!