Tarifas de inscripción de Swissdamed
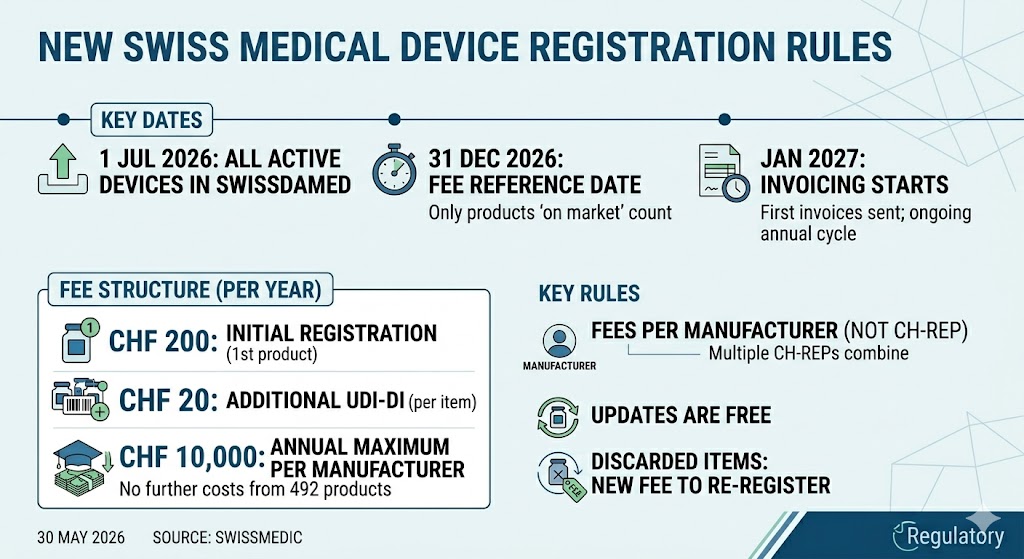
Nuevo requisito de registro para productos sanitarios: lo que se aplica a partir de julio de 2026 A partir del 1 de julio de 2026, los productos sanitarios en el…

Nuevo requisito de registro para productos sanitarios: lo que se aplica a partir de julio de 2026 A partir del 1 de julio de 2026, los productos sanitarios en el…
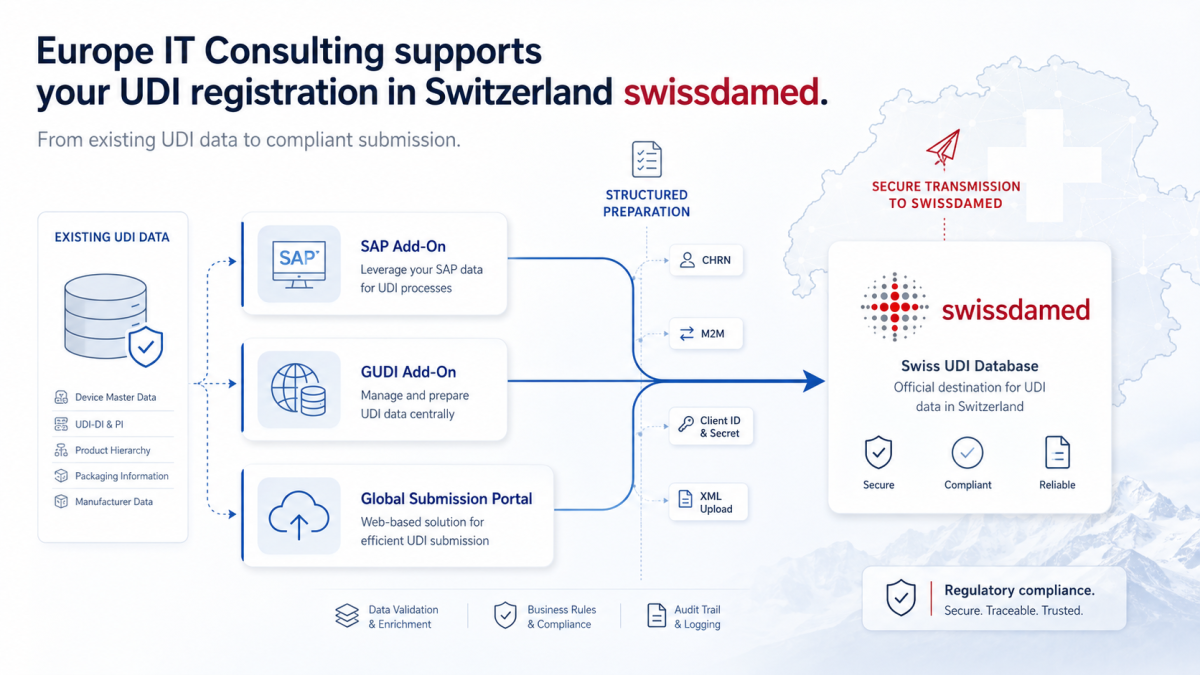
swissdamed: Cómo Europe IT Consulting apoya el registro UDI en Suiza Con swissdamed, Swissmedic está ampliando sistemáticamente la base de datos nacional para productos sanitarios y productos de diagnóstico in…

Fecha límite de EUDAMED: 28 de mayo de 2026: Cuando una nueva UDI-DI adelanta el registro de la Basic UDI-DI En pocas semanas, el 28 de mayo de 2026, el…
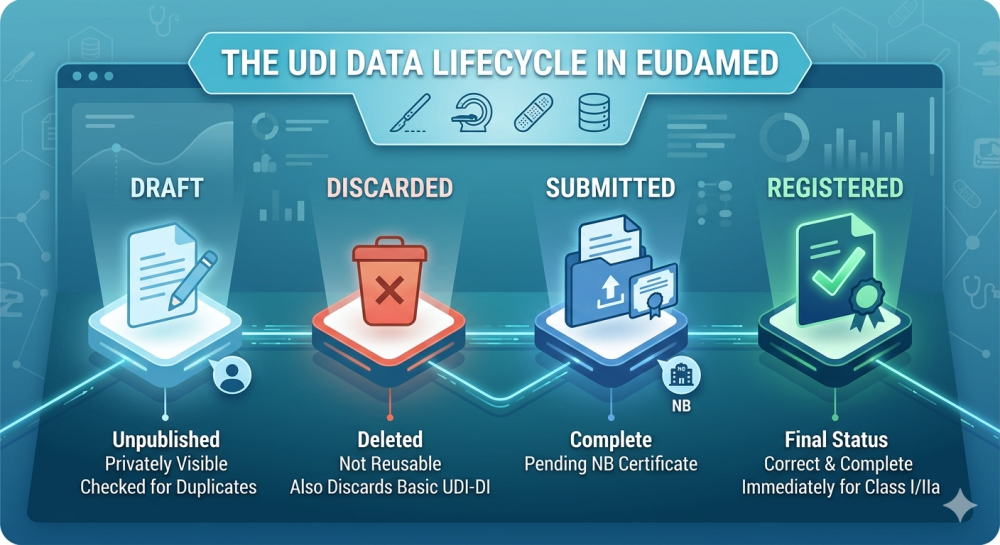
Estado de EUDAMED ¿Qué significan Draft, Discarded, Submitted y Registered en los datos UDI? Cualquier persona que gestione datos UDI en EUDAMED o los transmita a través de XML o…
2026 aumenta la presión de actuación para los fabricantes 2026 será un año operativamente exigente para muchas empresas de MedTech. En la UE, los primeros cuatro módulos de EUDAMED pasarán…
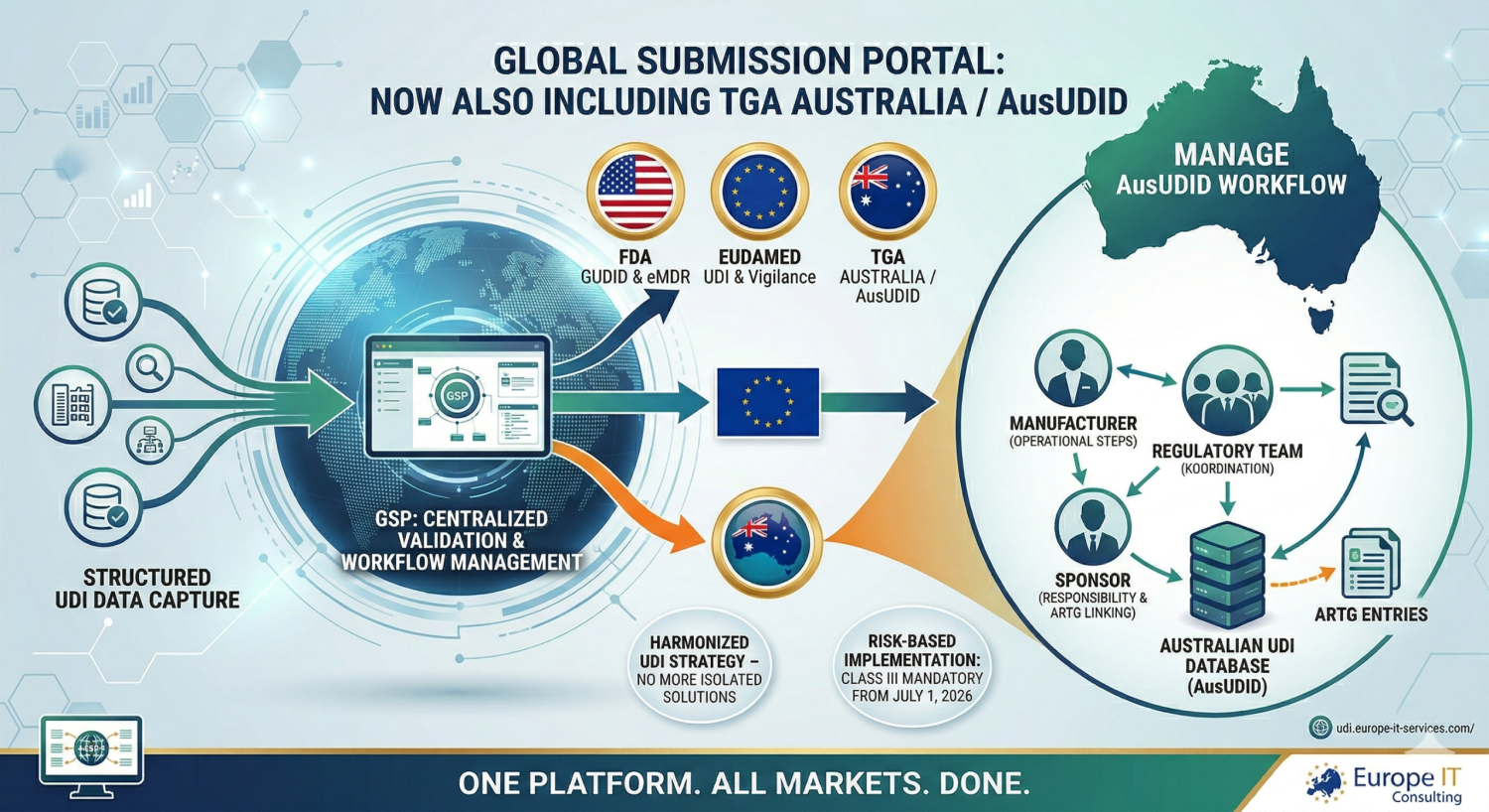
Australia en el GSP: Registrar datos UDI de forma estructurada, validarlos y gestionarlos de manera centralizada para el flujo de trabajo de AusUDID El Global Submission Portal sigue creciendo: tras…
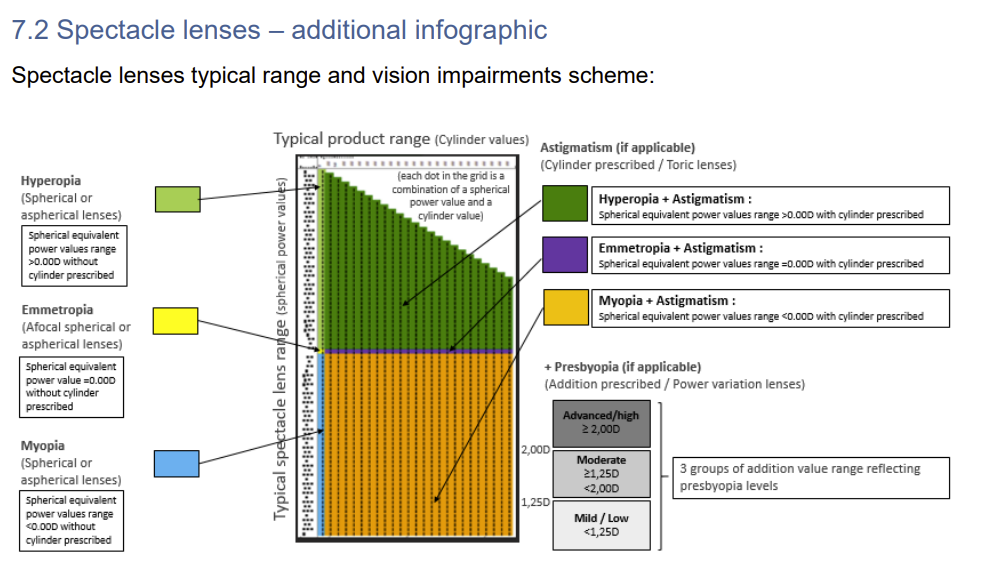
Publicada la nueva directriz del MDCG sobre el UDI-DI Maestro para monturas de gafas, lentes oftálmicas y gafas de lectura premontadas Con el documento MDCG 2025-8 Rev. 1, el Grupo…

regularia 2026: conversaciones personales, fuertes impulsos del mercado y valiosas perspectivas para la práctica regulatoria digital Una vez más, regularia 2026 demostró hasta qué punto la industria de la tecnología…
Gestión de datos en EUDAMED: Europe IT Consulting GmbH detecta fuentes críticas de error en las actualizaciones de UDI Los expertos de Europe IT Consulting GmbH han identificado una vulnerabilidad…
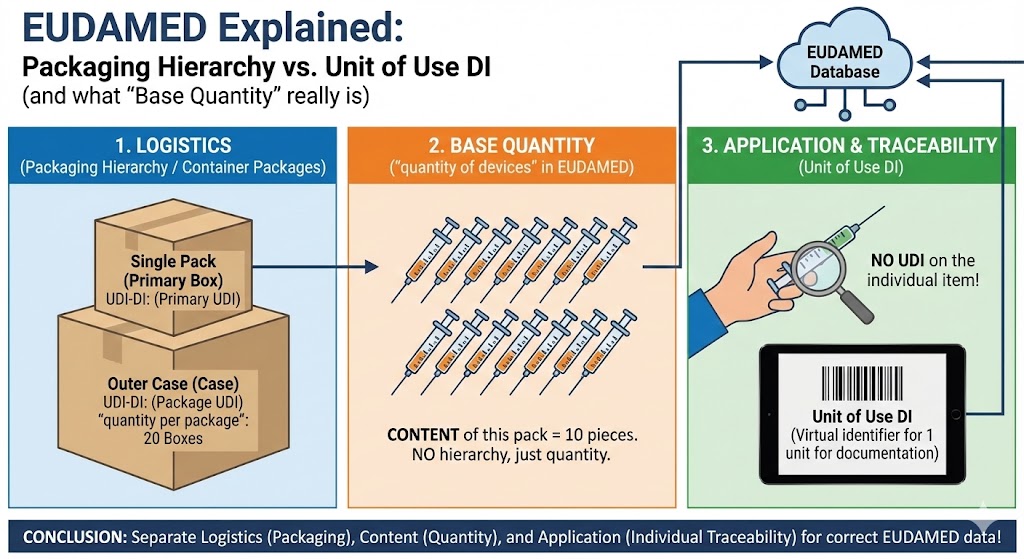
EUDAMED explicado de forma sencilla: Jerarquía de envasado vs. Unit of Use DI (y qué es realmente la „Base Quantity“) En EUDAMED, tres temas se confunden con especial frecuencia: la…