La solución inteligente para una gestión estructurada de datos UDI de AusUDID
Prepare sus datos UDI para la Australian UDI Database de forma estructurada, verificable y eficiente.
Su problema es nuestra solución
Con la Australian Unique Device Identification Database, abreviada como AusUDID, la Therapeutic Goods Administration (TGA) introduce una base de datos UDI central para productos sanitarios y productos sanitarios de diagnóstico in vitro comercializados en Australia. Para fabricantes, patrocinadores y otras organizaciones implicadas, esto supone un nuevo reto operativo: los datos UDI deben prepararse, comprobarse y presentarse de forma completa, coherente y conforme a los requisitos de la TGA.
Nuestra plantilla Excel para AusUDID le ofrece el primer paso estructurado: desarrollada por expertos en UDI para empresas que desean preparar eficientemente sus datos UDI australianos y evitar errores de validación posteriores.
Por favor, complete el formulario para solicitar una oferta
La plantilla Excel UDI de AusUDID de un vistazo:
La plantilla está dividida en pestañas de entrada especializadas y listas técnicas de códigos.
El registro real de datos se realiza en las pestañas A a F. Las pestañas con el prefijo “CL_” contienen listas de códigos y valores de selección que sirven como ayuda de entrada y base de validación. Esto garantiza que la entrada de datos no se realice de forma libre e incontrolada, sino mediante valores predefinidos y una lógica de selección regulatoriamente relevante.
A-AusUDID – Pestaña principal central para el registro UDI
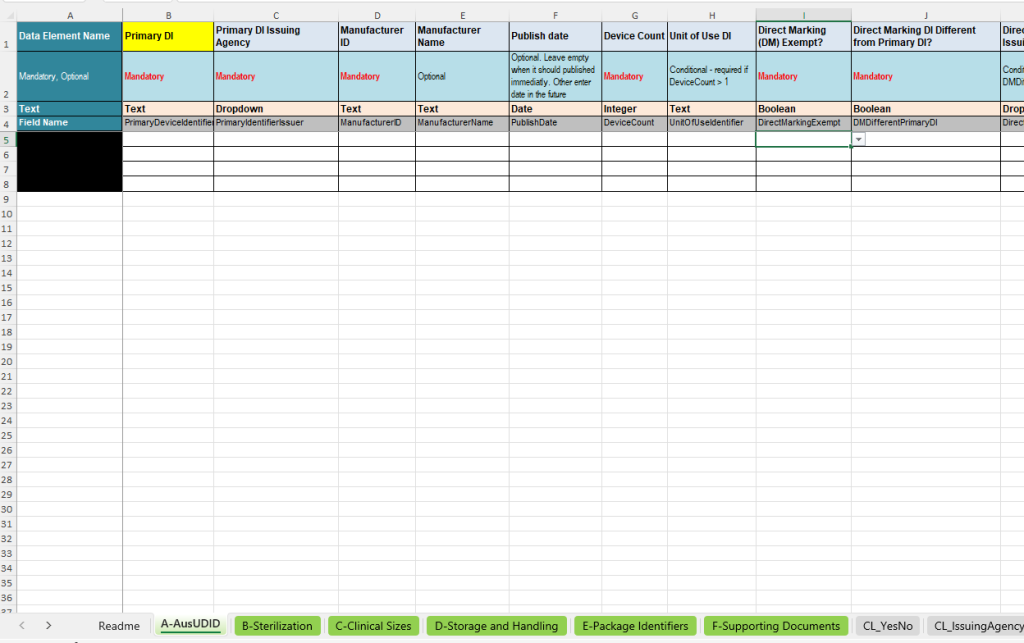
La pestaña A-AusUDID es la pestaña principal central de la plantilla. Aquí se mantienen los datos maestros más importantes de un registro UDI. El Primary Device Identifier constituye la clave central mediante la cual las pestañas adicionales se vinculan con el producto correspondiente.
- Primary Device Identifier: Identificador central del dispositivo para la identificación inequívoca del producto.
- Primary DI Issuing Agency: Indicación de la entidad emisora, por ejemplo GS1, HIBCC o ICCBBA.
- Manufacturer ID y Manufacturer Name: Identificación y nombre del fabricante.
- Publish Date: Fecha de publicación opcional, si el registro no debe publicarse inmediatamente.
- Device Count y Unit of Use DI: Registro del número de productos incluidos y, si es necesario, del identificador Unit-of-Use.
- Direct Marking: Información sobre si se requiere marcado directo, si existe una excepción y si se utiliza un Direct Marking DI diferente.
- Brand Name y Model/Version: Nombre del producto, modelo o versión.
- Device Class: Selección de la clase de riesgo australiana, por ejemplo Class III, Class IIb, Class IIa, Class I o clases IVD.
- Información sobre software y kits: Indicación de si se trata de software, Software as a Medical Device o un kit.
- Device Description y GMDN Code: Descripción del producto y asignación a la Global Medical Device Nomenclature.
- ARTG ID, Catalogue Number y Sponsor Commercial Distribution End Date: Información sobre la vinculación con el Australian Register of Therapeutic Goods, así como datos de distribución relacionados con el patrocinador.
- MRI Safety Status: Clasificación de la seguridad en resonancia magnética, por ejemplo MR Safe, MR Conditional o MR Unsafe.
- Single Use y Reuse: Información sobre uso único y, en su caso, reutilización limitada.
- Etiquetado sobre látex y caucho natural: Registro de información relevante de etiquetado sobre látex o caucho natural.
- Esterilidad y esterilización: Información sobre si el producto está envasado estérilmente o debe esterilizarse antes de su uso.
- Production Identifier: Indicación de si el lote, la fecha de fabricación, el número de serie, la fecha de caducidad o el Donation ID Number figuran en la etiqueta.
- Secondary DI y Previous DI: Documentación de identificadores de dispositivo adicionales o anteriores, incluida la entidad emisora correspondiente.
Beneficio: Esta pestaña principal crea la base central de datos para la presentación en AusUDID. Agrupa toda la información esencial sobre producto, fabricante, etiquetado, clasificación e identificación en una tabla estructurada.
Por favor, complete el formulario para solicitar una oferta
B-Sterilization – Métodos de esterilización
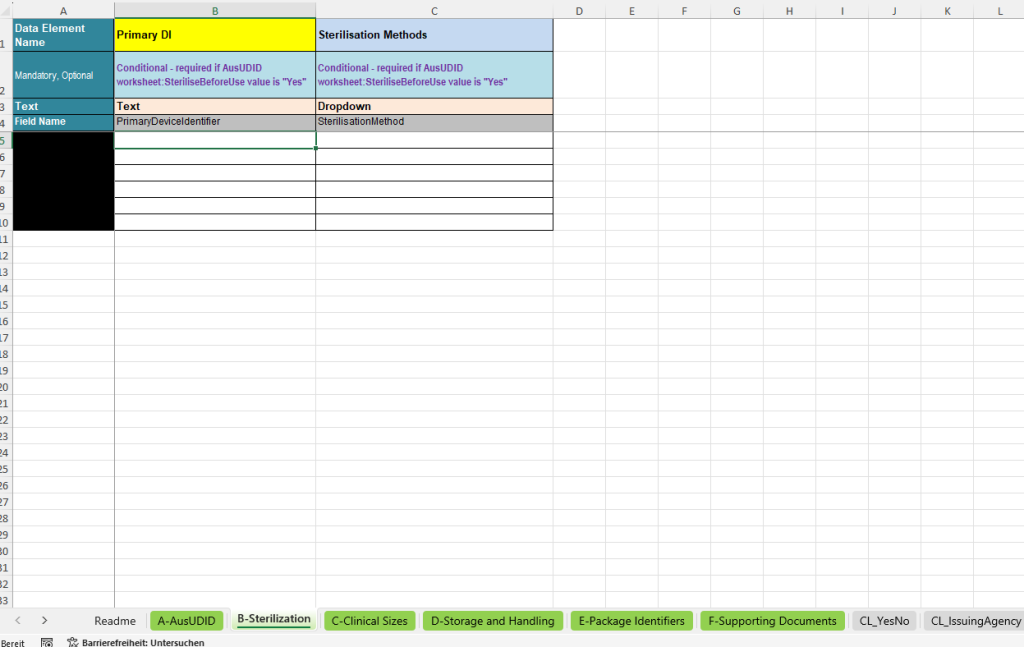
La pestaña B-Sterilization se utiliza cuando en la pestaña principal se ha indicado que el producto debe esterilizarse antes de su uso. En este caso, los métodos de esterilización relevantes deben registrarse de forma estructurada para el Primary Device Identifier correspondiente.
- Primary DI: Vinculación con el registro UDI correspondiente de la pestaña principal.
- Sterilisation Methods: Selección del método de esterilización aplicable mediante una lista de selección definida.
La plantilla admite diferentes métodos de esterilización, como por ejemplo óxido de etileno, esterilización por vapor, calor seco, radiación gamma, haz de electrones, peróxido de hidrógeno, plasma u otros procedimientos.
Beneficio: La información sobre esterilización no se mantiene de forma no estructurada en la pestaña principal, sino en una pestaña propia. Esto permite asignar correctamente varios métodos relevantes al producto correspondiente.
C-Clinical Sizes – Información sobre tamaños clínicos
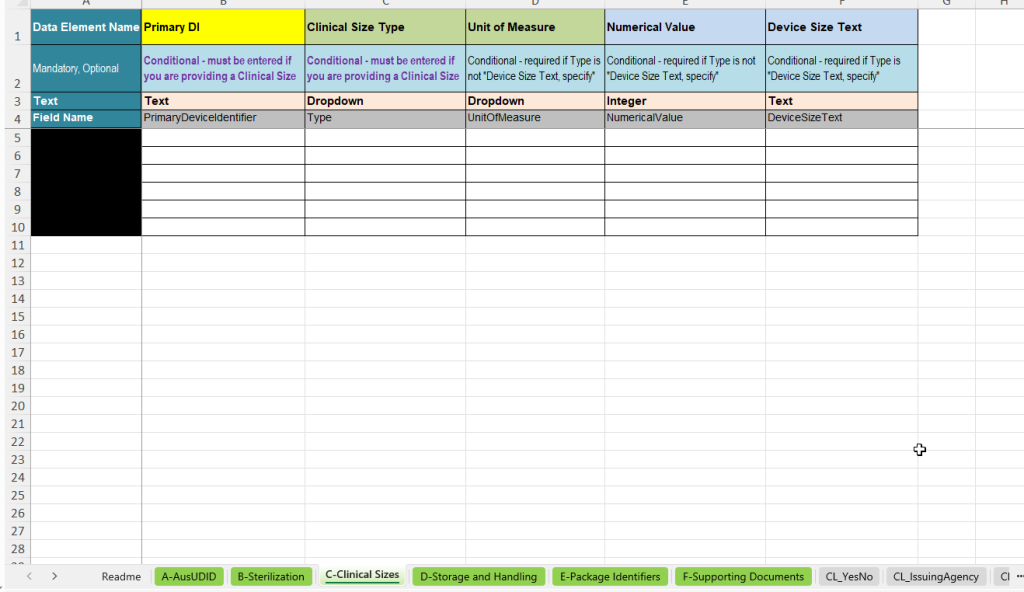
La pestaña C-Clinical Sizes sirve para registrar información clínicamente relevante sobre tamaños. Se utiliza cuando deben o pueden indicarse el tamaño del producto, sus dimensiones u otras características de tamaño relevantes para la notificación de datos AusUDID.
- Primary DI: Vinculación con el registro UDI correspondiente.
- Clinical Size Type: Selección del tipo de tamaño, por ejemplo longitud, superficie, ángulo, gauge u otras categorías de tamaño.
- Unit of Measure: Unidad de medida, por ejemplo milímetro, centímetro, pulgada, grado u otras unidades.
- Numerical Value: Valor numérico del tamaño.
- Device Size Text: Campo de texto libre si el tamaño no puede representarse adecuadamente de forma numérica o debe indicarse como texto específico.
La plantilla distingue entre tamaños numéricos y tamaños expresados únicamente como texto. Si se indica un tamaño estandarizado con unidad, se mantienen el tipo, la unidad y el valor. Si el tamaño solo puede representarse de forma razonable como texto, se utiliza el campo Device Size Text.
Beneficio: Los tamaños clínicos se registran de forma coherente y evaluable. Al mismo tiempo, la plantilla mantiene la flexibilidad necesaria para productos cuyas dimensiones no pueden representarse exclusivamente de forma numérica.
D-Storage and Handling – Condiciones de almacenamiento y manipulación
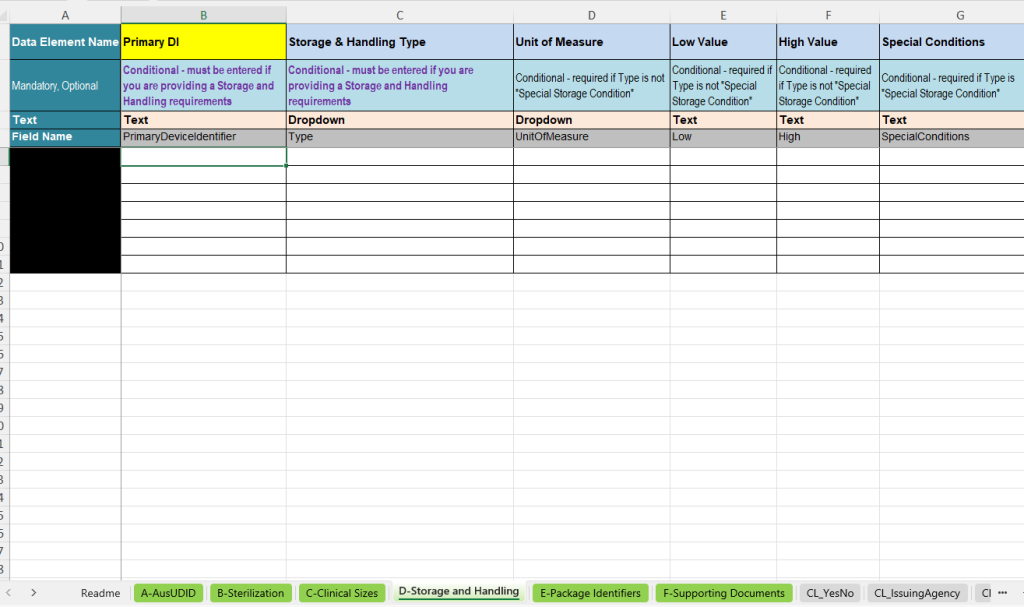
La pestaña D-Storage and Handling documenta requisitos especiales de almacenamiento y manipulación del producto. Esta información es importante cuando deben respetarse determinadas condiciones ambientales o indicaciones especiales para el almacenamiento y el transporte.
- Primary DI: Asignación de la condición al registro UDI correspondiente.
- Storage & Handling Type: Selección del tipo de condición, por ejemplo temperatura, humedad, presión atmosférica o condición especial de almacenamiento.
- Unit of Measure: Unidad para la condición correspondiente, por ejemplo grados Celsius, Fahrenheit, Kelvin, porcentaje de humedad relativa, kPa o mbar.
- Low Value y High Value: Valor límite inferior y superior para la condición correspondiente.
- Special Conditions: Campo de texto libre para condiciones especiales cuando no se utilizan valores límite numéricos.
La plantilla contiene una lógica en la que se utilizan valores límite numéricos y unidades cuando se trata de condiciones medibles. Para condiciones especiales de almacenamiento, puede mantenerse en su lugar una descripción textual.
Beneficio: Los datos críticos de almacenamiento y manipulación se registran de forma estructurada y pueden comprobarse por producto. Esto ayuda a evitar indicaciones de texto libre poco claras y valores límite contradictorios.
Por favor, complete el formulario para solicitar una oferta
E-Package Identifiers – Identificadores de envase y jerarquía de embalaje
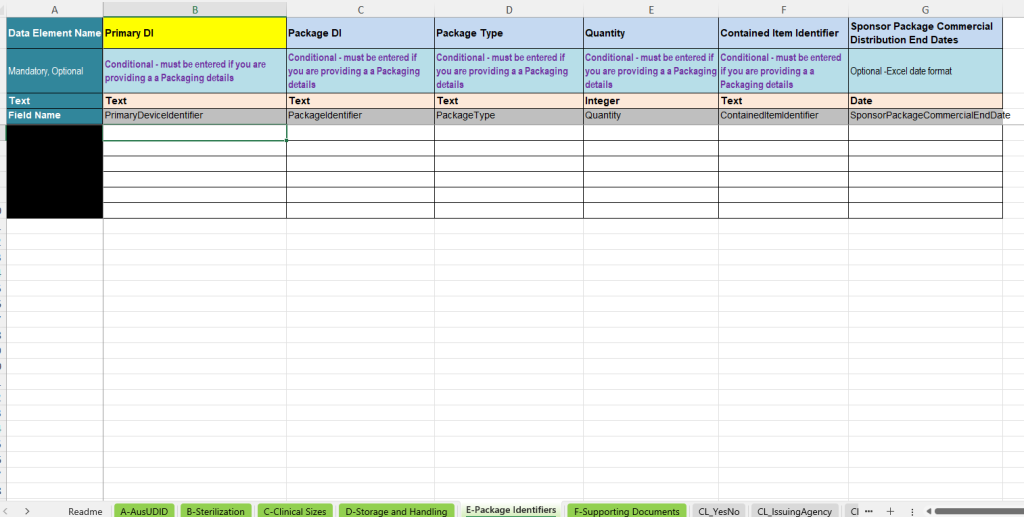
La pestaña E-Package Identifiers sirve para registrar identificadores adicionales de envase e información sobre embalaje. Es especialmente relevante cuando, además del Primary Device Identifier, deben documentarse otros niveles de embalaje o unidades contenidas.
- Primary DI: Vinculación con el registro principal.
- Package DI: Identificador de la unidad de embalaje.
- Package Type: Tipo de unidad de embalaje, por ejemplo nivel de embalaje o forma de embalaje.
- Quantity: Número de unidades contenidas.
- Contained Item Identifier: Identificador del producto o de la unidad contenida.
- Sponsor Package Commercial Distribution End Date: Fecha opcional de finalización de la distribución comercial para el nivel de embalaje.
Beneficio: Las estructuras de embalaje no se describen únicamente como texto, sino como una relación trazable entre el identificador de envase, el producto contenido y la cantidad. Esto es especialmente importante en embalajes multinivel, sets o grandes carteras de productos.
F-Supporting Documents – Documentos de apoyo
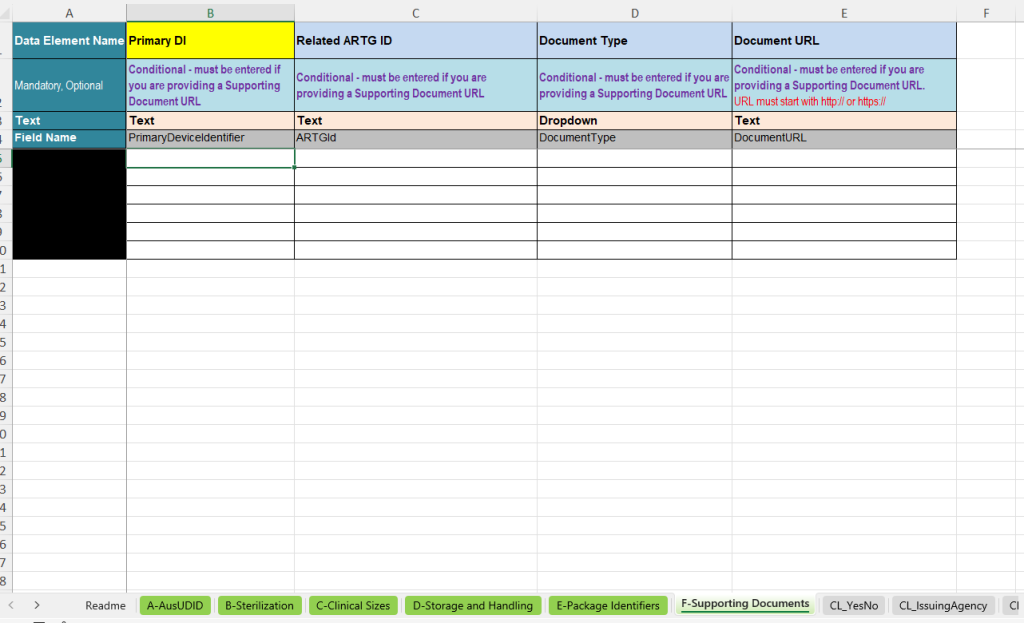
La pestaña F-Supporting Documents se utiliza cuando deben indicarse documentos relacionados con el producto mediante una URL. Esto incluye, por ejemplo, instrucciones de uso o folletos de información para pacientes.
- Primary DI: Vinculación con el registro UDI correspondiente.
- Related ARTG ID: Referencia al ARTG ID relevante.
- Document Type: Selección del tipo de documento, por ejemplo Instructions for Use o Patient Information Leaflet.
- Document URL: Dirección web del documento. La URL debe comenzar .
Beneficio: Los documentos de apoyo se vinculan de forma estructurada con el registro UDI y la referencia ARTG. Esto aumenta la trazabilidad y facilita la disponibilidad de información relacionada con el producto.
Readme – Instrucciones y lógica de edición
La pestaña Readme contiene indicaciones generales sobre el uso de la plantilla. Explica, entre otras cosas, que deben completarse todas las hojas de Excel relevantes y que las pestañas con el prefijo “CL_” sirven como listas de códigos y ayuda de entrada.
- No añadir ni eliminar columnas: La estructura de la plantilla no debe modificarse para garantizar un procesamiento posterior sin errores.
- Campos obligatorios: Los campos marcados en rojo deben completarse.
- Campos opcionales: Pueden completarse si la información está disponible o es técnicamente pertinente.
- Campos obligatorios condicionales: Deben completarse cuando se cumpla la condición correspondiente.
- Campos de fecha: Las fechas deben introducirse como valores reales de fecha en Excel.
Beneficio: La pestaña Readme reduce errores de uso y garantiza que los usuarios comprendan la lógica de la plantilla antes de comenzar con el registro de datos.
Pestañas CL – Listas de códigos y valores de selección controlados
Las pestañas con el prefijo CL_ no son pestañas normales de entrada, sino listas de códigos controladas. Sirven como base para campos desplegables, valores de selección estandarizados y terminología uniforme dentro de la plantilla.
- CL_YesNo: Valores estandarizados de Sí/No y N/A.
- CL_IssuingAgency: Entidades emisoras UDI compatibles, como GS1, HIBCC e ICCBBA.
- CL_Device Class: Clases de riesgo australianas para productos sanitarios e IVD.
- CL_HandlUnitOfMeasures: Unidades y tipos para condiciones de almacenamiento y manipulación.
- CL_Sterilization: Lista controlada de métodos de esterilización.
- CL_SupportingDocs: Tipos de documentos como Patient Information Leaflet o Instructions for Use.
- CL_DeviceIsSoftware: Valores de selección para Software as a Medical Device, producto sanitario con software o “No”.
- CL_MRISafety: Valores sobre seguridad en resonancia magnética, por ejemplo MR Safe, MR Conditional y MR Unsafe.
- CL_ClinicUnitOfMeasures: Amplia lista de unidades y tipos para información sobre tamaños clínicos.
Beneficio: Las listas de códigos reducen el texto libre, mejoran la calidad de los datos y apoyan un procesamiento técnico coherente. Los usuarios seleccionan valores de listas controladas en lugar de introducir términos manualmente y potencialmente de forma inconsistente.
Por favor, complete el formulario para solicitar una oferta
Funciones inteligentes para la máxima eficiencia
- Separación clara de pestañas: Datos maestros, esterilización, tamaños clínicos, condiciones de almacenamiento, embalajes y documentos se mantienen por separado.
- Primary DI como clave: La información adicional se vincula de forma inequívoca con el registro principal mediante el Primary Device Identifier.
- Lógica de campos obligatorios y condicionales: La plantilla distingue entre campos obligatorios, campos opcionales e información requerida de forma condicional.
- Entrada asistida por listas desplegables: Las listas de códigos apoyan entradas estandarizadas y reducen desviaciones.
- Preparación para la validación: La plantilla estructurada facilita la revisión antes de la preparación técnica o presentación.
- Escalabilidad: Adecuada tanto para productos individuales como para amplias carteras UDI.
Oferta integral de servicios para su cumplimiento con AusUDID
- Plantilla Excel UDI para AusUDID: La base profesional para el registro estructurado de sus datos UDI para Australia.
- Revisión y validación de datos: Le apoyamos en la revisión especializada de sus datos UDI para que las inconsistencias típicas puedan detectarse y corregirse en una fase temprana.
- Preparación técnica: Los datos Excel estructurados pueden utilizarse como base para conversión técnica, procesos de carga o preparación M2M.
- Servicio de transmisión AusUDID: Acompañamos el proceso desde el registro de datos y la revisión hasta la preparación y el apoyo para la presentación en AusUDID.
Especificaciones técnicas de la plantilla Excel
- Formato de archivo: Microsoft Excel (.xlsx)
- Compatibilidad: Microsoft Excel 2016 y versiones posteriores
- Estructura: Una pestaña principal, cinco pestañas adicionales especializadas y varias listas de códigos
- Validación de datos: Listas desplegables y listas de valores controlados para entradas coherentes
- Lógica de clave: Vinculación de las pestañas adicionales mediante el Primary Device Identifier
- Actualizaciones: Adaptación de la plantilla en caso de cambios relevantes en los requisitos de datos o especificaciones técnicas
Por favor, complete el formulario para solicitar una oferta
Por qué las empresas líderes de tecnología médica confían en nuestra solución
Europe IT Consulting GmbH es su socio para soluciones informáticas regulatorias, gestión de datos UDI y transmisiones técnicas de datos. Ayudamos a las empresas a preparar datos UDI complejos de forma estructurada y a utilizarlos eficientemente para bases de datos regulatorias.
Esto es lo que hace única a nuestra plantilla Excel para AusUDID:
- Estructuración precisa de los elementos de datos relevantes para AusUDID
- Separación clara entre el registro principal y la información adicional especializada
- Listas de códigos controladas para entradas estandarizadas
- Reducción de errores de validación mediante una lógica de campos predefinida
- Preparación óptima para revisión manual, conversión técnica y procesos M2M
- Uso orientado a la práctica para Regulatory Affairs, gestión de calidad, IT y socios externos
- ANALIZAR: Identifique qué datos AusUDID son relevantes para sus productos.
- ESTRUCTURAR: Registre sus datos UDI en una lógica clara de pestañas.
- VALIDAR: Compruebe campos obligatorios, campos condicionales y valores de selección controlados.
- TRANSMITIR: Utilice los datos estructurados como base para preparación técnica, carga o procesos M2M.
Perfectamente adaptada a sus requisitos individuales
Para carteras de productos pequeñas y medianas:
La plantilla Excel ofrece una base clara para el registro estructurado de datos y la revisión posterior.
Para grandes carteras UDI:
La estructura separada por pestañas ayuda a preparar limpiamente incluso grandes volúmenes de datos de producto y a mantener información adicional relacionada con cada producto.
Para empresas con datos existentes de FDA-GUDID o EUDAMED:
Los datos UDI existentes pueden utilizarse como punto de partida. No obstante, los datos deben revisarse técnicamente para AusUDID, adaptarse a los requisitos australianos y presentarse activamente.
Para procesos orientados a M2M:
El registro estructurado de datos constituye una base importante para la conversión técnica, la preparación HL7 SPL / XML y otros procesos de transmisión automatizados.
Preguntas frecuentes que facilitan su decisión
¿Puedo utilizar datos UDI existentes de otros mercados?
Sí, los datos UDI existentes de FDA GUDID, EUDAMED o datos maestros UDI internos pueden servir como base. Sin embargo, deben revisarse y complementarse conforme a los requisitos de AusUDID.
¿Puedo generar archivos M2M directamente con la plantilla Excel?
No, la plantilla Excel sirve principalmente para el registro estructurado de datos. Ofrecemos la conversión técnica a un formato de intercambio adecuado como servicio separado.
¿Por qué hay varias pestañas?
No toda la información pertenece al registro principal. Los métodos de esterilización, tamaños clínicos, condiciones de almacenamiento, identificadores de envase y documentos pueden aparecer varias veces o estar sujetos a condiciones. Las pestañas separadas permiten una estructura de datos limpia y escalable.
¿Qué papel desempeña el Primary Device Identifier?
El Primary Device Identifier es la clave central. A través de él, la información de las pestañas adicionales se asigna de forma inequívoca al producto correcto.
¿Qué son las pestañas CL?
Las pestañas CL son listas de códigos. Contienen valores controlados para campos desplegables, por ejemplo clases de riesgo, entidades emisoras, métodos de esterilización, estado de seguridad MRI o unidades de medida.
¿Qué ocurre si se añade o elimina una columna?
La estructura no debe modificarse. Columnas adicionales o eliminadas pueden afectar al procesamiento técnico posterior y al proceso de carga.
¿Quién debe completar la plantilla?
Normalmente colaboran Regulatory Affairs, gestión de calidad, gestión de datos maestros, IT y, en su caso, el patrocinador australiano. Muchos campos requieren coordinación técnica entre el fabricante y el patrocinador.
Actúe ahora: prepare sus datos AusUDID con antelación.
Los requisitos UDI australianos serán obligatorios de forma gradual. Las empresas que estructuran, validan y preparan técnicamente sus datos UDI con antelación reducen ciclos posteriores de corrección, riesgos de carga y cuellos de botella operativos.
Su primer paso hacia un cumplimiento AusUDID eficiente:
Por favor, complete el formulario para solicitar una oferta
Invierta ahora en una estrategia estructurada de datos regulatorios para Australia.
La plantilla Excel UDI para AusUDID es desarrollada y distribuida por Europe IT Consulting GmbH, su socio certificado para soluciones informáticas regulatorias desde 2011.
Nota: Antes de iniciar el proyecto, revise los requisitos, plazos, roles, exigencias de datos y especificaciones técnicas actualmente vigentes de la TGA. Los datos UDI existentes de otros mercados pueden servir como punto de partida, pero no sustituyen la revisión técnica ni la presentación activa en AusUDID.