Descripción general de UDI EUDAMED
Con el nuevo Reglamento de Dispositivos Médicos (MDR 2017/745) y el Reglamento de Dispositivos de Diagnóstico In Vitro (IVDR 2017/746) de la Comisión Europea, se introdujeron nuevos requisitos para los dispositivos médicos. La Identificación Única de Dispositivos (UDI) tiene como objetivo identificar globalmente los dispositivos médicos para mejorar la trazabilidad, la transparencia y la seguridad del paciente.
Impacto de UDI en los fabricantes de dispositivos médicos
Para colocar dispositivos médicos en el mercado europeo, las empresas de dispositivos médicos deben cumplir con estas nuevas regulaciones, incluida la implementación de UDI. El UDI específico del producto debe mantenerse y enviarse a la Base de Datos Europea de Dispositivos Médicos (EUDAMED). Cada dispositivo médico debe asignarse a un UDI-DI básico y necesita un UDI-DI único.
Cronograma de implementación de UDI
La introducción de las nuevas regulaciones médicas afecta en gran medida a la mayoría de las empresas de dispositivos médicos y a su cartera de productos. Por esta razón, el cumplimiento de UDI se establece sucesivamente y se planea implementarlo para 2027. De este modo, la prioridad se establece de acuerdo con la clase de riesgo de los dispositivos médicos.

Plan de proyecto UDI
Para cumplir con los requisitos de las nuevas regulaciones MDR e IVDR, hemos elaborado una hoja de ruta paso a paso que lo ayuda en su camino hacia el cumplimiento de UDI.

Integración técnica UDI
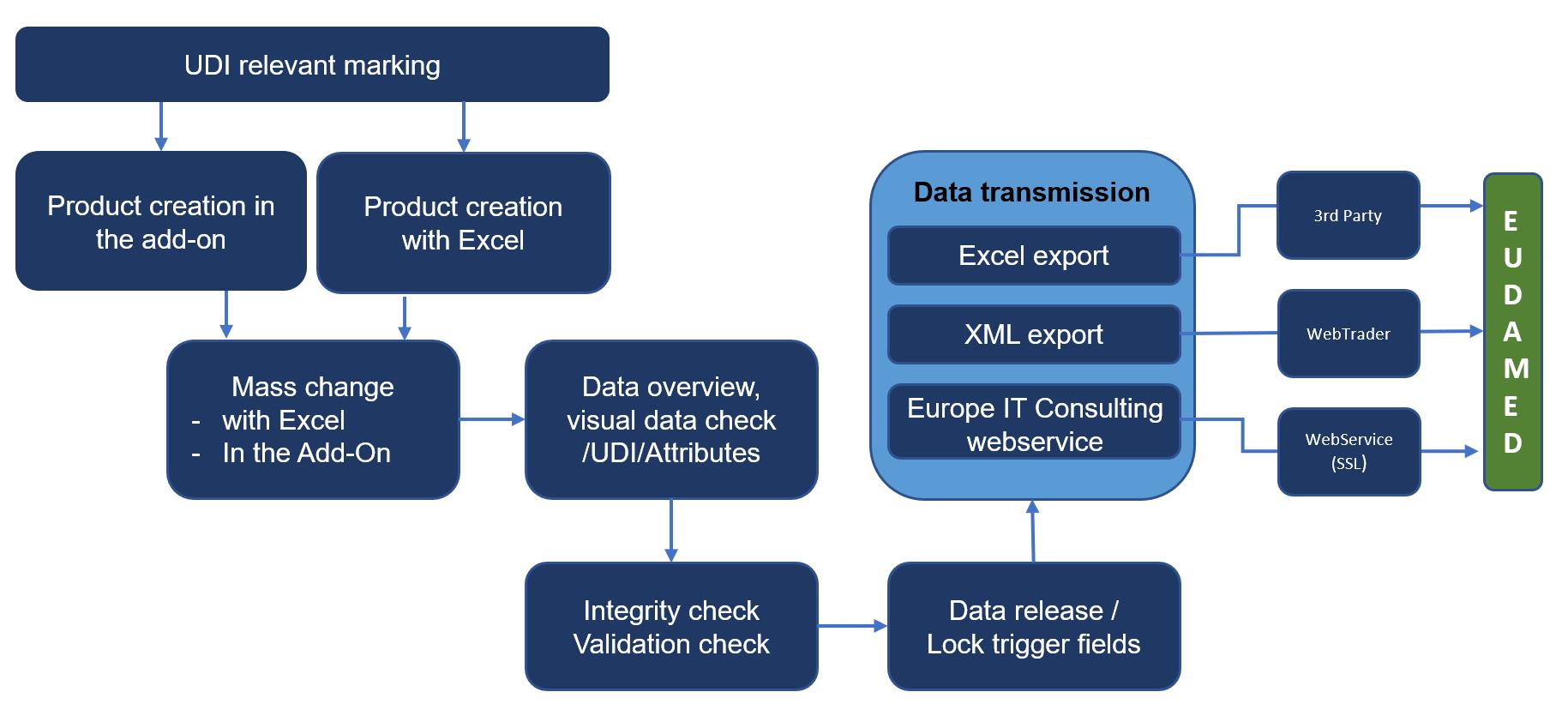
Para una gestión de datos UDI eficaz y eficiente, hemos desarrollado un complemento UDI EU SAP. Esta solución le ayuda a mantener, gestionar y enviar sus datos UDI a EUDAMED, todo en un solo sistema. La siguiente ilustración representa el proceso de gestión de datos UDI en la solución UDI EU SAP Add-On.
Gestión de datos UDI
Nuestras soluciones para EUDAMED:
https://www.europe-it-consulting.ch/index.php/eudamed-mdr-ivdr-excel-template/?lang=es
https://www.europe-it-consulting.ch/index.php/udi-eudamed-solution-as-sap-add-on/?lang=es
Si desea obtener más información sobre la implementación de UDI, nuestras soluciones técnicas y servicios de UDI, no dude en ponerse en contacto con nosotros en cualquier momento.