Australia en el GSP:
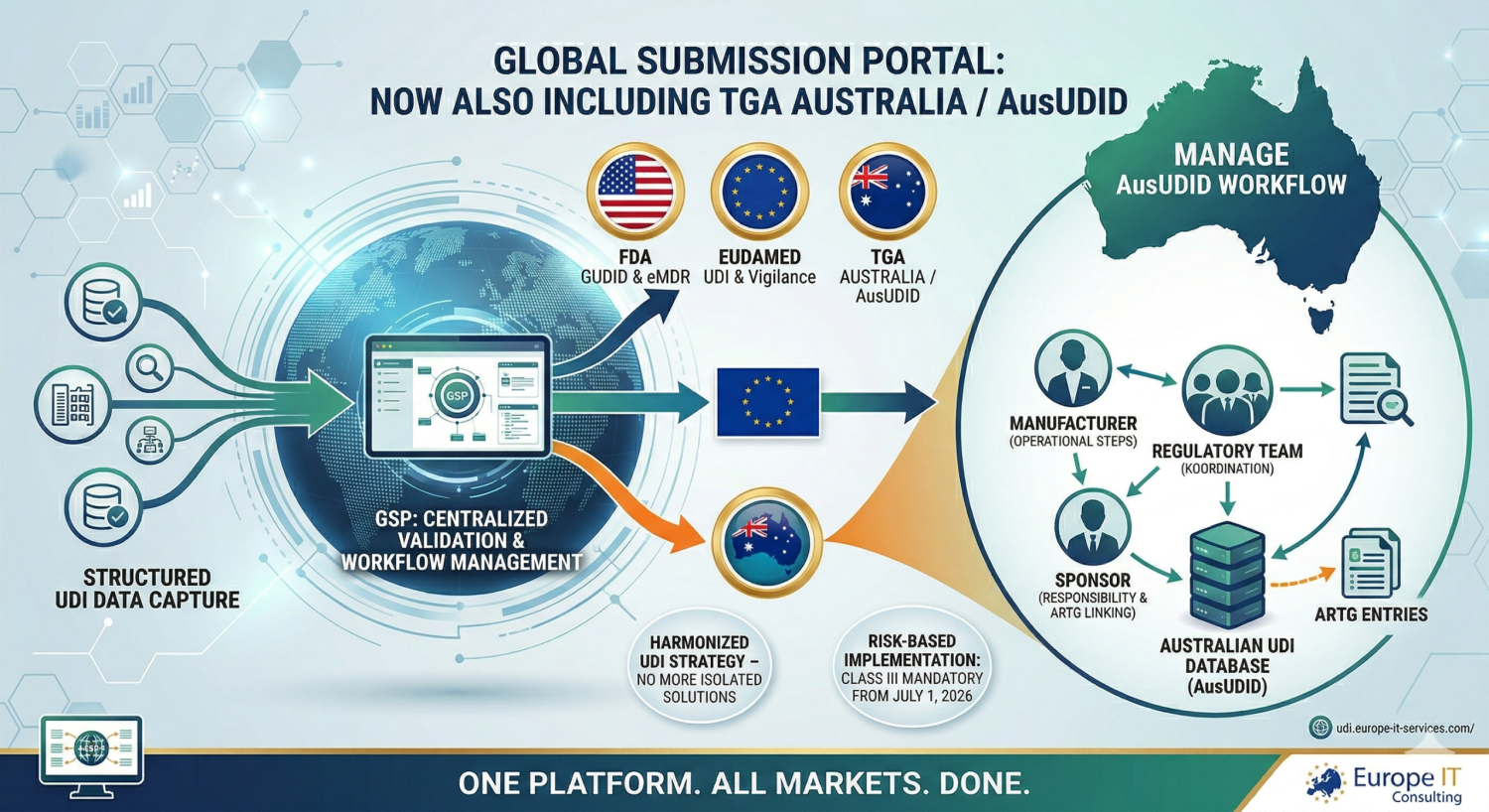
Registrar datos UDI de forma estructurada, validarlos y gestionarlos de manera centralizada para el flujo de trabajo de AusUDID
El Global Submission Portal sigue creciendo: tras su lanzamiento con FDA eMDR, FDA GUDID y EUDAMED UDI, así como su ampliación para incluir EUDAMED Vigilance, ahora también damos soporte a Australia. Esto convierte al GSP en una plataforma central aún más sólida para los procesos globales de presentación regulatoria.
Este momento ha sido elegido deliberadamente. Australia introdujo su sistema UDI a nivel regulatorio ya en 2025, la Australian UDI Database (AusUDID) ya está activa, y su implementación se está llevando a cabo de forma escalonada y basada en el riesgo durante varios años. Para los fabricantes y sponsors de dispositivos médicos de Clase III y Clase IIb, la UDI será obligatoria a partir del 1 de julio de 2026; las demás clases seguirán en los años posteriores.
AusUDID: Base central de datos para el mercado australiano
Con AusUDID, la TGA está creando una base central de datos para los UDI-DI y los datos de producto asociados en Australia. Los conjuntos de datos UDI publicados se vinculan con las entradas ARTG correspondientes.
Precisamente aquí es donde entra en juego el Global Submission Portal: ayuda a preparar de forma estructurada los datos relevantes para UDI, a organizar mejor los procesos de revisión y aprobación, y a trasladar los flujos de presentación a un entorno uniforme.
Australia como parte de la estrategia global de UDI
Esto es especialmente importante para las empresas MedTech con presencia internacional: Australia ya no es un caso aislado, sino otro mercado que debe integrarse en la estrategia global de UDI. Quienes ya gestionan procesos de FDA o EUDAMED se benefician de un enfoque armonizado, en lugar de añadir más soluciones aisladas.
Precisamente esta estandarización es el enfoque del GSP:
- menos rupturas de medios
- mayor transparencia
- seguimiento de estado más claro
- y un mejor control operativo de las presentaciones regulatorias
Lógica de roles en Australia: sponsor, fabricante, equipo regulatorio
Desde el punto de vista regulatorio, la lógica de roles en Australia es importante: los sponsors siguen siendo responsables de la presentación y del mantenimiento de los registros UDI. Aunque los fabricantes pueden asumir muchos pasos operativos en AusUDID, la vinculación con el ARTG sigue siendo relevante del lado del sponsor. Para las empresas con estructuras internacionales, por tanto, no solo es decisiva la captura de datos, sino también un flujo de trabajo bien gestionado entre fabricante, sponsor y equipo regulatorio.
Una plataforma. Todos los mercados. Listo.
Con la ampliación para incluir TGA Australia / AusUDID, Europe IT Consulting sigue desarrollando de forma consecuente el Global Submission Portal. El objetivo sigue siendo el mismo: hacer que los procesos globales de presentación para las empresas MedTech sean más claros, más robustos y más eficientes, todo en un solo sistema.
Envíe su solicitud directamente aquí: https://udi.europe-it-services.com/





Related Posts