
Regularia 2026 el 3 de marzo en el Ayuntamiento de Tuttlingen
El programa ya está online – visite a Europe IT Consulting en el Stand 12
El 3 de marzo de 2026 se celebrará por primera vez en el Stadthalle Tuttlingen regularia, el nuevo foro regulatorio para la tecnología médica. El programa ya se ha publicado: MDR, cumplimiento de materiales (Material Compliance), digitalización de RA y GC, aprobaciones internacionales, así como Ciberseguridad / Software / Ley de IA (AI Act). Estaremos presentes como expositores mostrando en vivo cómo hacer los procesos de UDI y de envío de datos (submission) mucho más eficientes.
regularia reúne a expertos y directivos de Asuntos Regulatorios, Gestión de Calidad, la política y la industria, con dos escenarios paralelos y una zona de exposición. El organizador ha publicado el programa del día y la información sobre las entradas; el registro y la descarga del programa están disponibles online.
Los bloques temáticos cubren los «puntos críticos» típicos del día a día regulatorio: cuestiones prácticas del MDR, cumplimiento de materiales (p. ej., PFAS / cambios en ISO), digitalización de RA y GC, aprobaciones internacionales, así como Ciberseguridad / Software / Ley de IA.
[Haga clic aquí para ver el resumen del programa]
Europe IT Consulting in situ
En nuestro stand mostraremos de forma práctica cómo dominar el camino desde la «preparación de datos» hasta la «transferencia a las autoridades», incluyendo validación, monitorización de estado y pruebas fiables (Audit-Trail).
Dos caminos, un resultado (Demostración en vivo en el stand)
-
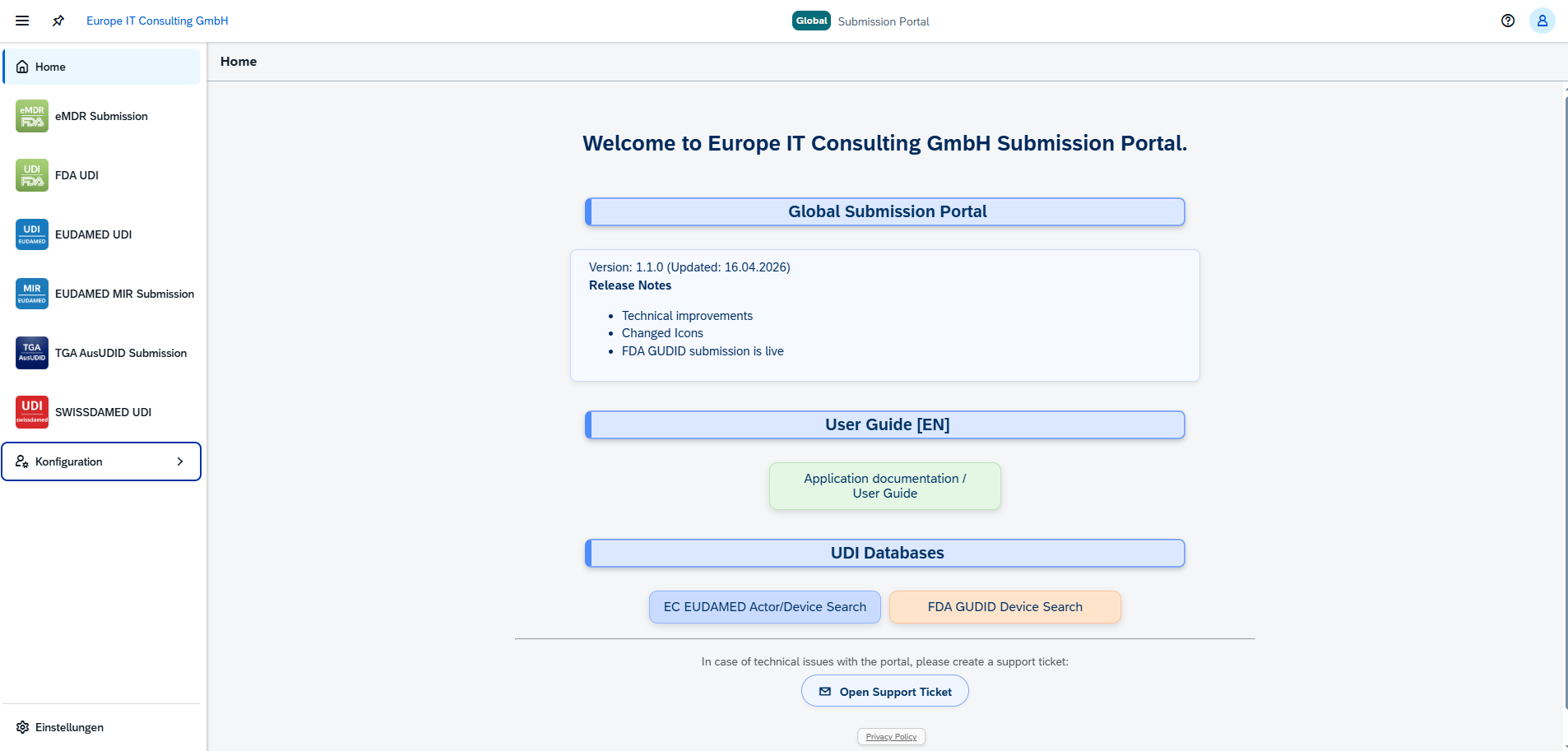
Global Submission Web Portal (Carga de Excel) Para equipos que quieren empezar rápidamente: cargar Excel, validar y transferir, sin necesidad de un proyecto de TI e independientemente del sistema ERP.
-
SAP Global UDI Add-On (preparado para S/4HANA) Para empresas con SAP: gestión de datos UDI totalmente integrada, con control sobre procesos y datos, incl. conexión modular con autoridades (p. ej., EUDAMED / FDA / Swissdamed).
[Información oficial regularia y registro]
Si asiste a regularia, pase por nuestro stand y no dude en traer preguntas concretas o casos de uso (p. ej., registro EUDAMED-UDI, calidad de datos, procesos de envío, gestión de pruebas). Nos tomaremos el tiempo para una breve demostración en vivo y hablaremos sobre qué camino (Portal o SAP Add-On) se adapta mejor a sus necesidades.






Related Posts