Nos gustaría informarte hoy sobre los últimos avances respecto al módulo de Vigilancia en la base de datos EUDAMED.
Este módulo clave, cuya entrada en vigor está prevista para 2026, será esencial para que los fabricantes de dispositivos médicos cumplan con los requisitos normativos y garanticen la seguridad de sus productos.
¿Qué es el Módulo de Vigilancia de EUDAMED?
El módulo de Vigilancia de EUDAMED (Base de Datos Europea de Dispositivos Médicos) está diseñado para el registro y la notificación de incidentes graves de seguridad, eventos adversos y acciones correctivas de seguridad en el campo relacionadas con los dispositivos médicos.
Facilita una comunicación transparente y eficiente entre los fabricantes y las autoridades competentes en lo que respecta a la seguridad.
Obligaciones Regulatorias y Cumplimiento
Según el nuevo Reglamento de Dispositivos Médicos (MDR), el uso del módulo de Vigilancia será obligatorio para todos los fabricantes de dispositivos médicos.
Las empresas deben garantizar la notificación precisa y oportuna de todos los incidentes graves y acciones correctivas para evitar sanciones o restricciones en la distribución de productos.
Estructura del Módulo
El módulo de Vigilancia permitirá enviar informes electrónicamente a las autoridades competentes. Está dividido en varias secciones:
- Notificación de incidentes graves: Información detallada sobre eventos que pueden poner en riesgo la salud.
- Acciones correctivas de seguridad en el campo: Detalles de las medidas tomadas para mitigar los riesgos.
- Informes y retroalimentación: Herramientas para el seguimiento y la comunicación del estado de los informes.
¿Cuándo estará activo el Módulo de Vigilancia?
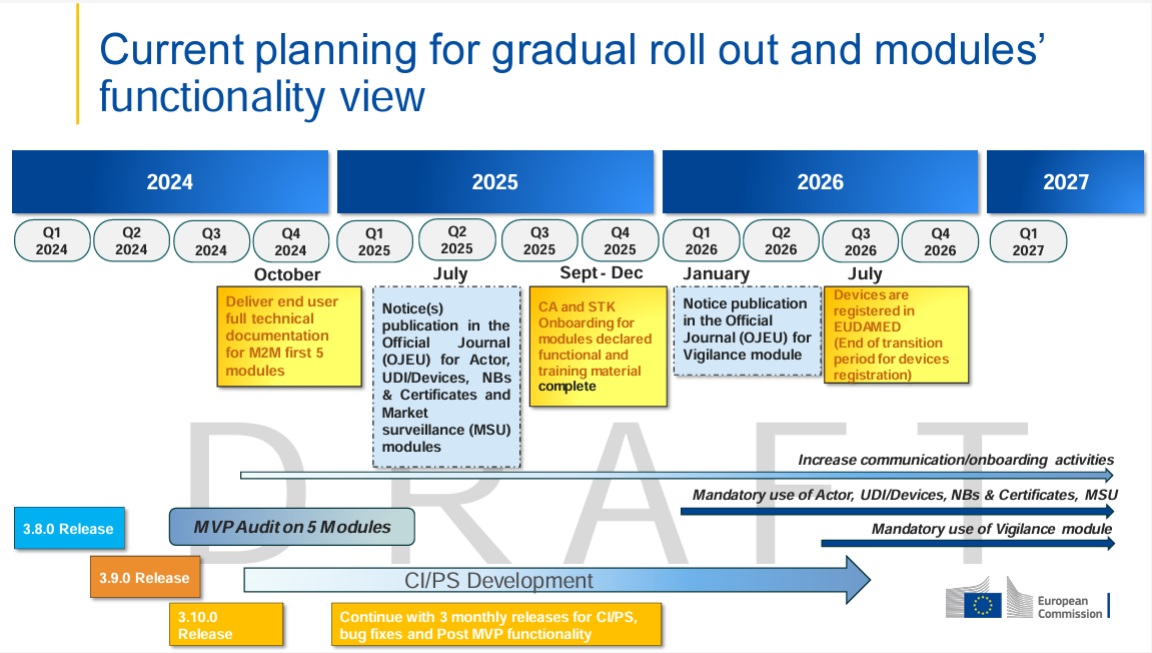
Se espera que el módulo esté operativo en el primer trimestre de 2026, y su uso obligatorio comenzará en el tercer trimestre de 2026.
Recomendamos prepararse con antelación para estos requisitos.
Próximos pasos:
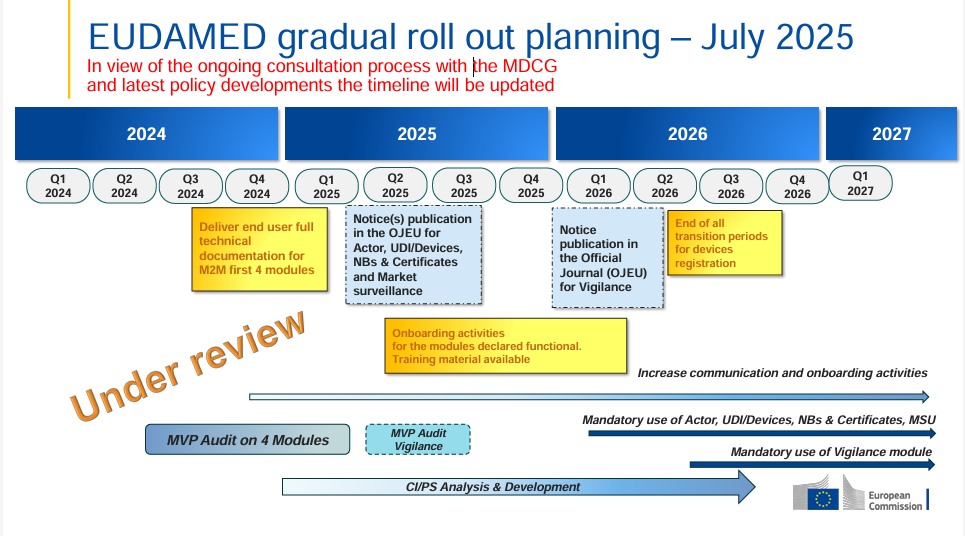
La Comisión Europea ha publicado una hoja de ruta que detalla el calendario y los hitos clave para la implementación de los distintos módulos de EUDAMED.
Asegúrate de revisar esta hoja de ruta para garantizar que tu empresa esté bien preparada.
👉 Haz clic aquí para ver la hoja de ruta.
Apoyo y Preparación
Para prepararte para la próxima entrada en vigor del módulo de Vigilancia, te recomendamos tomar las siguientes medidas:
✅ Revisar y optimizar los procesos internos para la notificación de incidentes.
✅ Capacitar al personal en los nuevos procesos de EUDAMED.
✅ Implementar una solución de software que facilite la recopilación de datos y la generación de informes, cumpliendo con los requisitos de EUDAMED.
Nuestro equipo está a tu disposición para ayudarte a implementar con éxito estas medidas.
Consecuencias del Incumplimiento
Los fabricantes que no cumplan con sus obligaciones se arriesgan a sanciones como multas o restricciones de venta en la UE.
Por ello, es fundamental cumplir con todos los requisitos a tiempo.
Una Primera Vista del Módulo de Vigilancia
Nos complace compartir contigo capturas de pantalla exclusivas del módulo de Vigilancia desde el entorno de pruebas de EUDAMED (EUDAMED Playground):
📸 (Aquí irían las imágenes si se incluyen en la versión final)







Related Posts