2026 aumenta la presión de actuación para los fabricantes
2026 será un año operativamente exigente para muchas empresas de MedTech. En la UE, los primeros cuatro módulos de EUDAMED pasarán a ser obligatorios a partir del 28 de mayo de 2026, concretamente Actor Registration, UDI/Device Registration, Notified Bodies & Certificates y Market Surveillance. En Suiza, el registro de productos, sistemas y procedure packs en swissdamed será obligatorio a partir del 1 de julio de 2026. Y en Australia, los requisitos obligatorios de UDI para los productos sanitarios de Clase III y Clase IIb también comenzarán el 1 de julio de 2026.
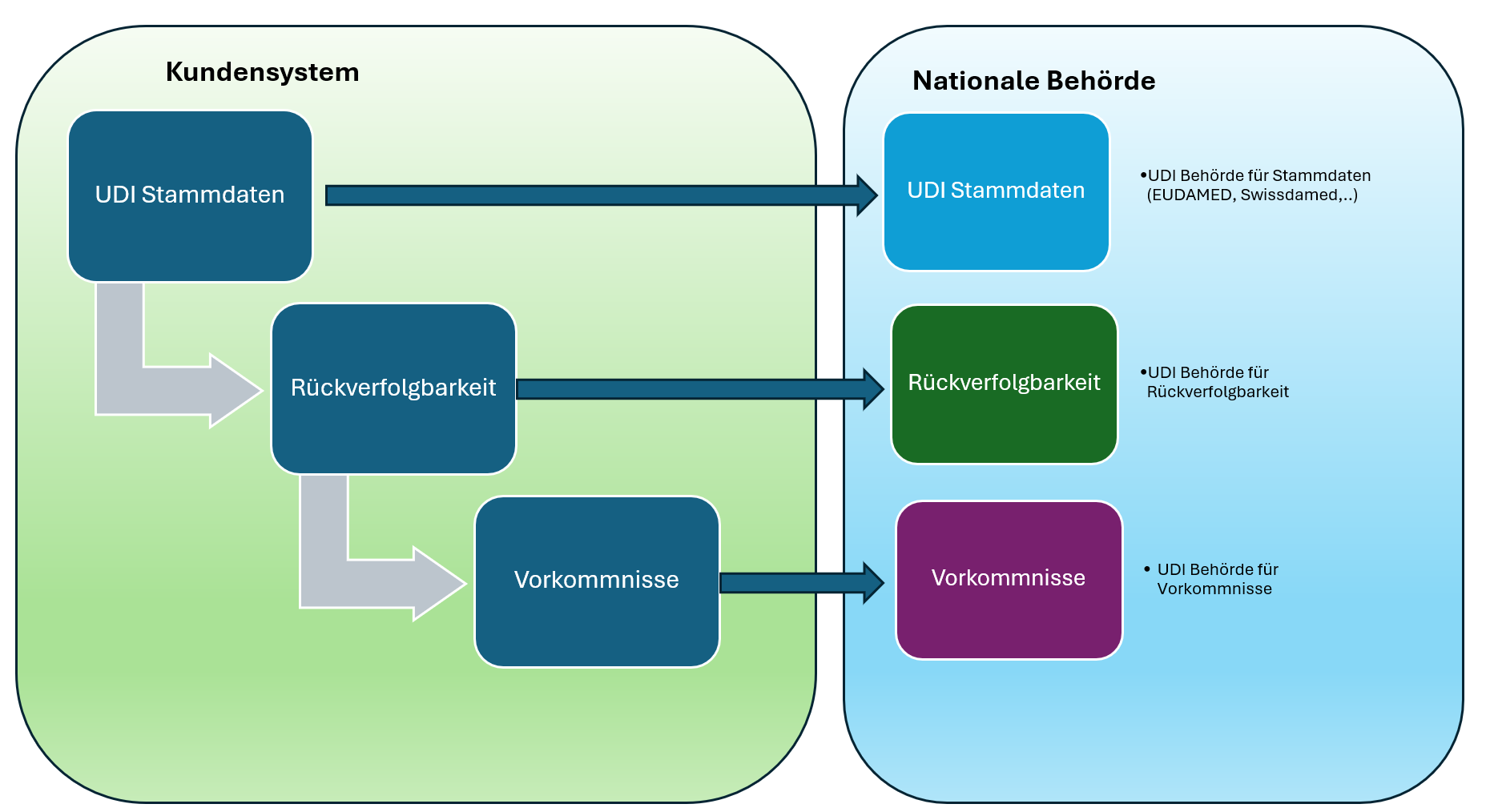
Con ello, la presión ya no aumenta solo en un mercado, sino de forma paralela en varios sistemas regulatorios. Para los fabricantes, esto significa que los datos UDI no solo deben existir, sino que también deben estar disponibles en una forma que permita validarlos, asignarlos y transmitirlos de manera estructurada y dentro de plazo. Quien siga trabajando con procesos aislados o con soluciones manuales independientes aumenta considerablemente el riesgo de retrasos, retrabajos y un esfuerzo de coordinación innecesario. Esta conclusión se deriva de las fechas de cumplimiento casi simultáneas en la UE, Suiza y Australia.
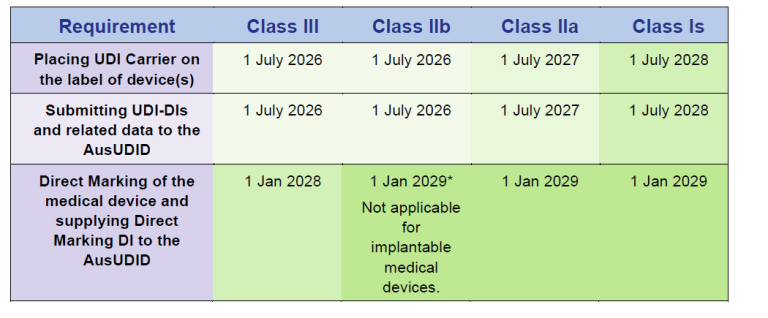
Australia 
En Australia, la presión de actuación es especialmente concreta. La TGA no solo exige el etiquetado UDI, sino también, entre otros aspectos, la transmisión de los datos UDI a la AusUDID, la vinculación con el ARTG ID, el mantenimiento continuo de los registros actualizados y, en el caso de los productos implantables, la inclusión de la UDI en la Patient Implant Card. Además, los datos UDI deben presentarse, por regla general, dentro de los 30 días siguientes al próximo suministro en Australia. Aunque los sponsors pueden designar a un tercero para ello, siguen siendo responsables de los datos presentados.
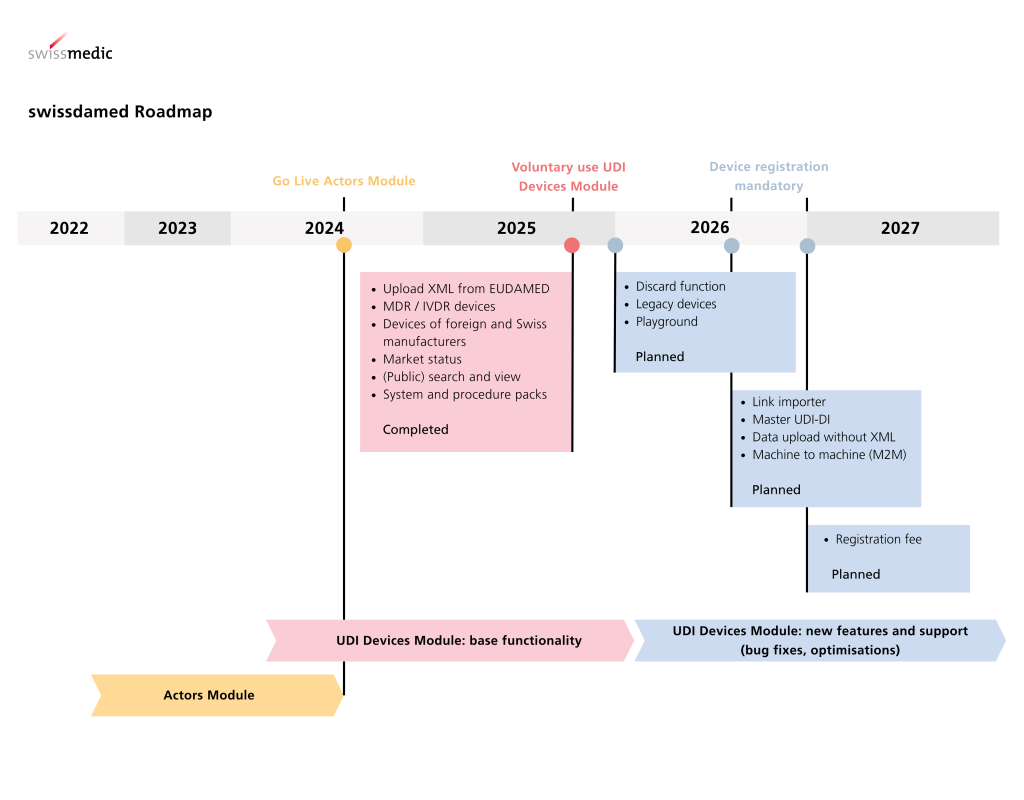
Suiza 
También en Suiza la dirección es clara. Swissmedic establece el 1 de julio de 2026 como fecha de inicio del registro obligatorio de productos en swissdamed y concede, en principio, un período transitorio hasta el 31 de diciembre de 2026. Al mismo tiempo, no existe período transitorio para determinados productos, en concreto allí donde deban notificarse a Swissmedic incidentes graves, field safety corrective actions o tendencias. Por ello, las empresas no deberían confiar únicamente en el año natural 2026, sino establecer con bastante antelación una lógica sólida de datos y de registro.
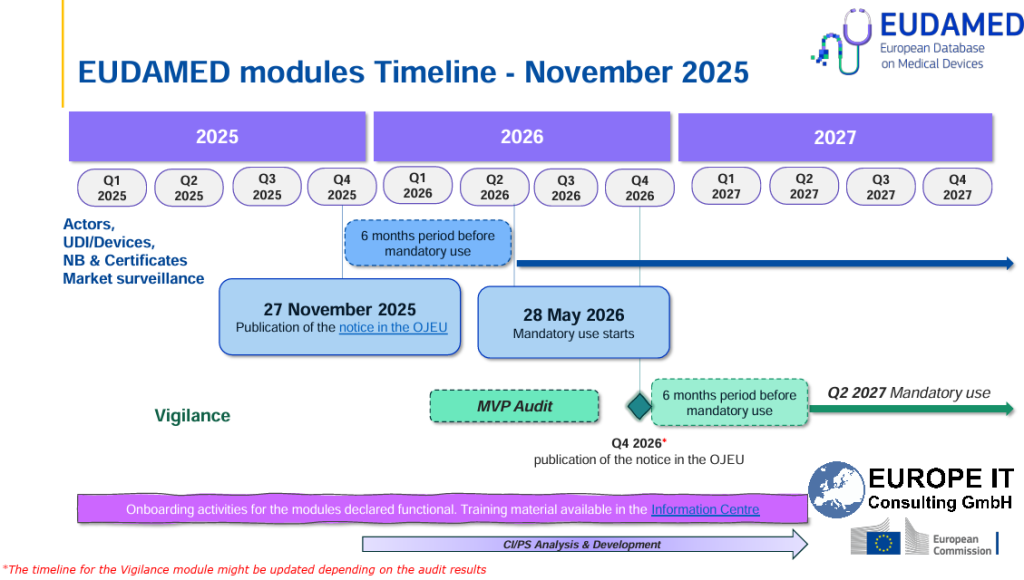
Unión Europea 
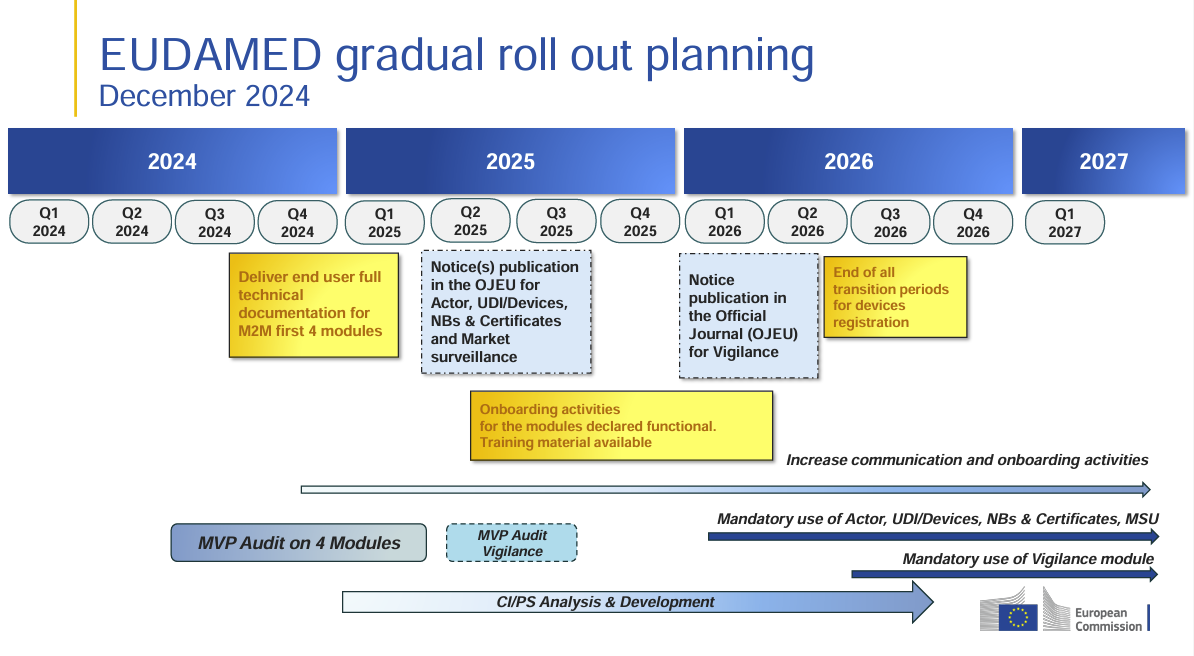
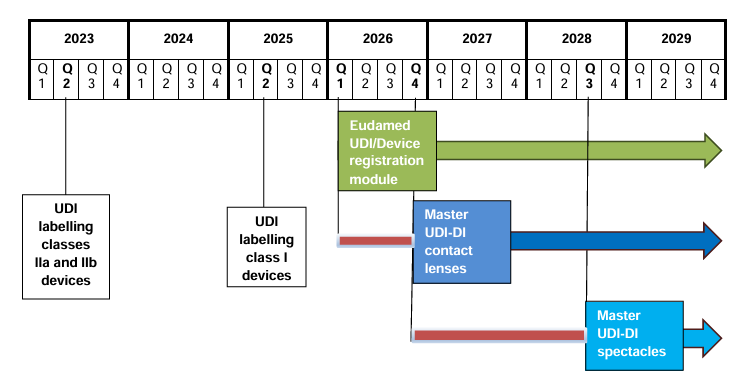
En la UE se añade además que EUDAMED pasa definitivamente de un funcionamiento voluntario a uno obligatorio. Tras la publicación de la decisión de funcionalidad a finales de noviembre de 2025, comenzó el período transitorio de seis meses, de modo que los primeros cuatro módulos serán obligatorios a partir del 28 de mayo de 2026. En este contexto, Swissmedic señala además que para los correspondientes registros en la UE existe un período transitorio hasta el 27 de noviembre de 2026. Esto aumenta aún más la presión sobre las empresas para no seguir gestionando sus datos de producto solo a nivel local o de forma ligada a proyectos, sino de manera apta para el mercado y preparada para la presentación regulatoria.
Global Submission Portal
Precisamente aquí es donde entra en juego nuestro Global Submission Portal. Europe IT Consulting introdujo inicialmente el portal para FDA eMDR, FDA GUDID y EUDAMED UDI, posteriormente lo amplió con EUDAMED Vigilance (MIR) y, más recientemente, incorporó también el flujo de trabajo para Swissmedic / swissdamed y TGA Australia / AusUDID. El beneficio es claro: captar los datos regulatorios de forma estructurada, validarlos y gestionarlos de manera centralizada para varios flujos de trabajo con autoridades, en lugar de crear nuevos procesos aislados para cada mercado.
Nuestra conclusión es, por tanto, inequívoca: 2026 no es un año para reaccionar tarde. Quien deba tener bajo control EUDAMED, swissdamed y Australia al mismo tiempo debería armonizar ya la calidad de los datos, las responsabilidades y los procesos de submission. Cuanto antes esté preparada esta base, menores serán las fricciones, los ciclos de corrección y los cuellos de botella operativos durante la implementación. Los plazos están fijados. Ahora lo que cuenta es la ejecución.
¿Desea preparar sus datos UDI para EUDAMED, swissdamed y Australia de forma estructurada y reunirlos en un proceso de submission coherente? Hable con nosotros sobre el enfoque adecuado para sus productos, mercados y fuentes de datos.







Related Posts