2026 erhöht den Handlungsdruck für Hersteller
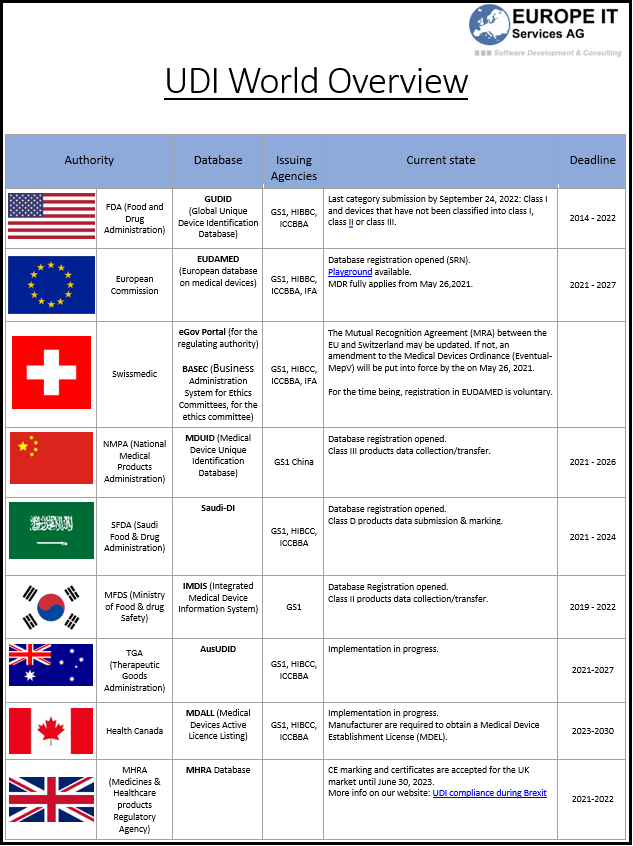
2026 ist für viele MedTech-Unternehmen operativ anspruchsvoll. In der EU werden ab 28. Mai 2026 die ersten vier EUDAMED-Module verpflichtend, nämlich Actor Registration, UDI/Device Registration, Notified Bodies & Certificates sowie Market Surveillance. In der Schweiz wird die Registrierung von Produkten, Systemen und Procedure Packs in swissdamed ab 1. Juli 2026 verpflichtend. Und in Australien beginnen die verbindlichen UDI-Anforderungen für Class III und Class IIb Medizinprodukte ebenfalls am 1. Juli 2026.
Damit steigt der Druck nicht nur in einem Markt, sondern parallel in mehreren regulatorischen Systemen. Für Hersteller bedeutet das: UDI-Daten müssen nicht nur vorhanden sein, sondern in einer Form bereitstehen, die sich strukturiert validieren, zuordnen und fristgerecht übermitteln lässt. Wer hier weiter mit isolierten Einzelprozessen oder manuell gepflegten Insellösungen arbeitet, erhöht das Risiko von Verzögerungen, Nacharbeit und unnötigem Abstimmungsaufwand deutlich. Diese Schlussfolgerung ergibt sich aus den nahezu zeitgleichen Pflichtterminen in EU, Schweiz und Australien.
Australien 
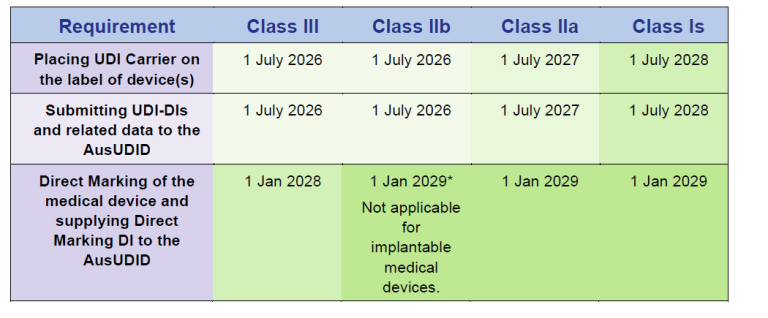
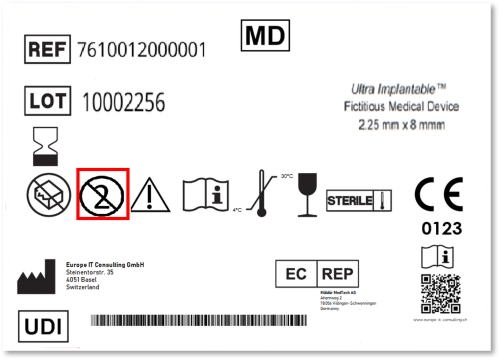
Besonders konkret wird der Handlungsdruck in Australien. Die TGA verlangt nicht nur die UDI-Kennzeichnung, sondern unter anderem auch die Übermittlung der UDI-Daten an die AusUDID, die Verknüpfung mit der ARTG ID, die laufende Pflege aktueller Datensätze sowie – bei implantierbaren Produkten – die Berücksichtigung der UDI auf der Patient Implant Card. Zudem müssen die UDI-Daten grundsätzlich innerhalb von 30 Tagen nach der nächsten Lieferung in Australien eingereicht werden. Sponsoren können dafür zwar einen Dritten einsetzen, bleiben jedoch weiterhin für die eingereichten Daten verantwortlich.
Schweiz 
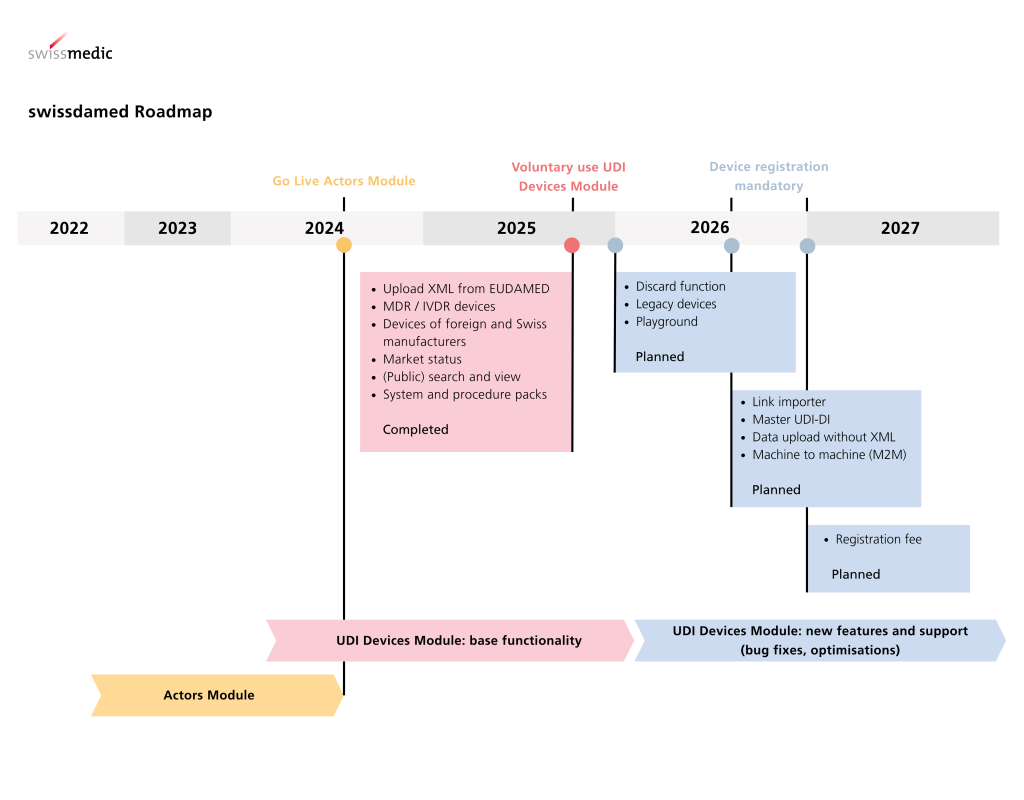
Auch in der Schweiz ist die Richtung eindeutig. Swissmedic nennt den 1. Juli 2026 als Start der obligatorischen Produktregistrierung in swissdamed und gewährt grundsätzlich eine Übergangsfrist bis 31. Dezember 2026. Gleichzeitig gilt für bestimmte Produkte keine Übergangsfrist, nämlich dort, wo schwerwiegende Vorkommnisse, Field Safety Corrective Actions oder Trends an Swissmedic gemeldet werden müssen. Unternehmen sollten sich deshalb nicht allein auf das Kalenderjahr 2026 verlassen, sondern ihre Daten- und Registrierungslogik deutlich früher belastbar aufsetzen.
Europäische Union 
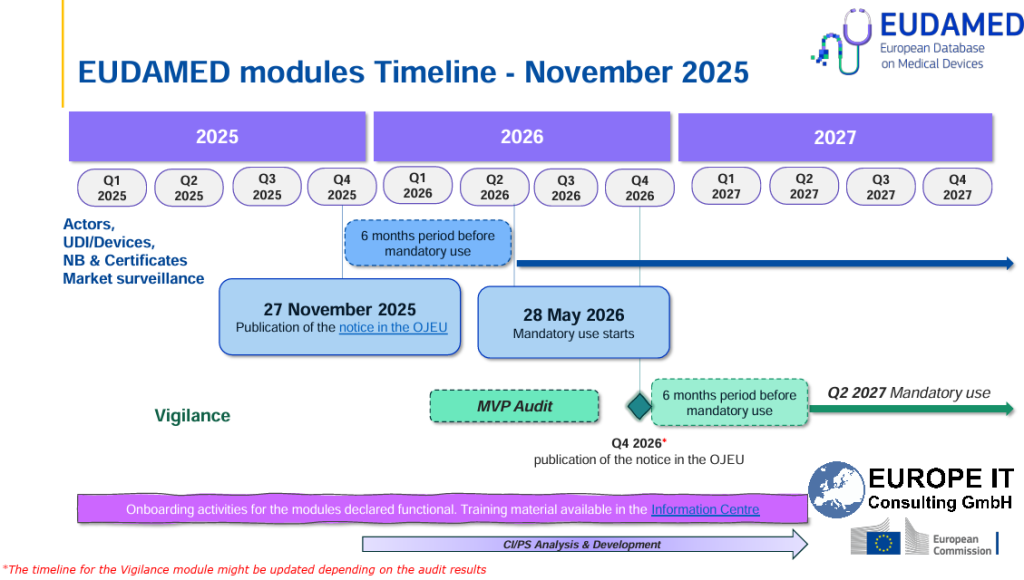
Für die EU kommt hinzu, dass EUDAMED damit endgültig vom freiwilligen in den verpflichtenden Betrieb übergeht. Nach Veröffentlichung der Funktionsentscheidung Ende November 2025 läuft die sechsmonatige Übergangsfrist, sodass die ersten vier Module ab 28. Mai 2026 verbindlich werden. Swissmedic verweist in diesem Zusammenhang zusätzlich darauf, dass für die entsprechenden EU-Registrierungen eine Übergangsfrist bis 27. November 2026 gilt. Auch das erhöht den Druck auf Unternehmen, ihre Produktdaten nicht mehr nur lokal oder projektbezogen zu verwalten, sondern marktfähig und submission-fähig vorzuhalten.
Global Submission Portal
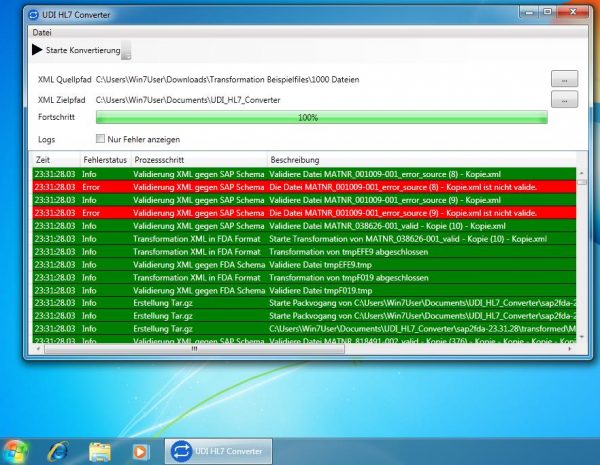
Genau hier setzt unser Global Submission Portal an. Europe IT Consulting hat das Portal zunächst für FDA eMDR, FDA GUDID und EUDAMED UDI eingeführt, anschließend um EUDAMED Vigilance (MIR) erweitert und zuletzt auch den Workflow für Swissmedic / swssidamed und TGA Australia / AusUDID aufgenommen. Der Nutzen ist klar: regulatorische Daten strukturiert erfassen, validieren und zentral für mehrere Behörden-Workflows steuern, statt für jeden Markt neue Einzelprozesse aufzubauen.
Unser Fazit ist daher eindeutig: 2026 ist kein Jahr für spätes Reagieren. Wer EUDAMED, swissdamed und Australien parallel im Blick behalten muss, sollte jetzt Datenqualität, Zuständigkeiten und Submission-Prozesse harmonisieren. Je früher diese Basis steht, desto geringer werden Reibungsverluste, Korrekturschleifen und operative Engpässe in der Umsetzung. Die Fristen sind gesetzt. Jetzt kommt es auf die Ausführung an.
Sie möchten Ihre UDI-Daten für EUDAMED, swissdamed und Australien strukturiert vorbereiten und in einem konsistenten Submission-Prozess zusammenführen? Sprechen Sie mit uns über den passenden Ansatz für Ihre Produkte, Märkte und Datenquellen.






Related Posts