
Fecha límite de EUDAMED: 28 de mayo de 2026:
Cuando una nueva UDI-DI adelanta el registro de la Basic UDI-DI
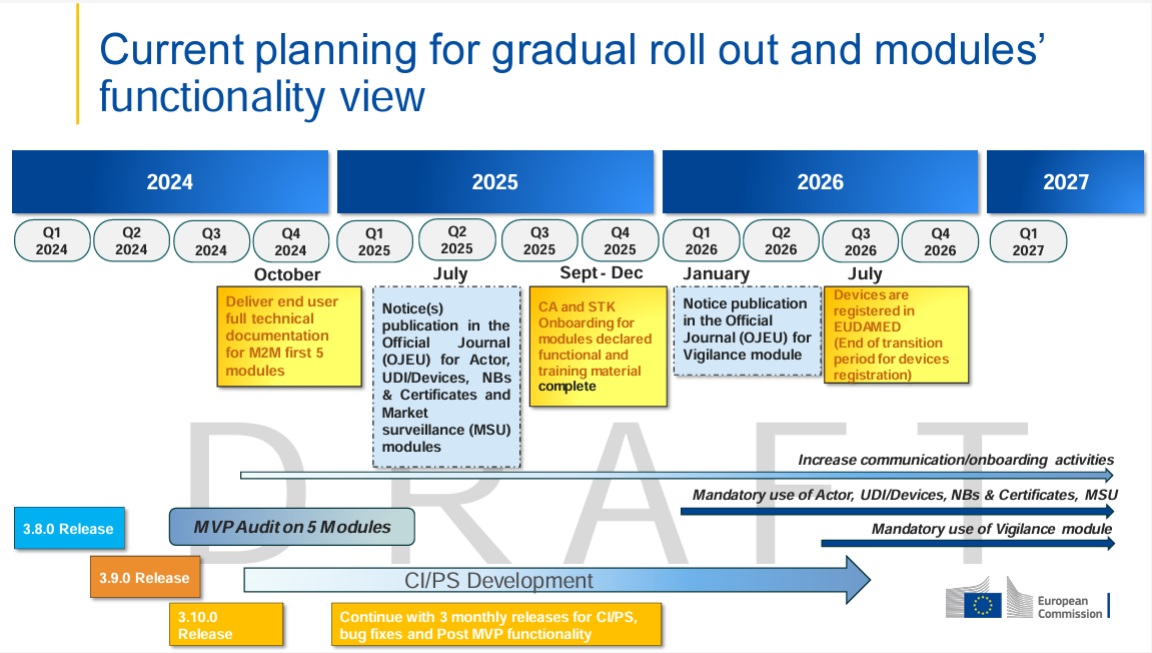
En pocas semanas, el 28 de mayo de 2026, el uso de los cuatro primeros módulos de EUDAMED será obligatorio. Entre ellos se encuentran, entre otros, el Actor Registration Module y el UDI/Devices Registration Module. Con la publicación de la Decisión de Ejecución (UE) 2025/2371, la Comisión Europea confirmó la funcionalidad de estos módulos; de ello se deriva su uso obligatorio a partir del 28 de mayo de 2026.
Muchos fabricantes han basado su planificación en el período transitorio adicional hasta el 27 de noviembre de 2026 para los productos que ya han sido introducidos en el mercado, y esto es, en principio, comprensible. Las preguntas y respuestas de la Comisión Europea sobre EUDAMED aclaran que, para los productos cuya primera unidad con una UDI-DI específica ya fue introducida en el mercado de la UE antes de la fecha de uso obligatorio del módulo UDI/Devices, el registro correspondiente debe completarse dentro de los doce meses siguientes a la publicación del aviso que confirma la funcionalidad.
Sin embargo, existe un escenario concreto que todavía no se tiene suficientemente en cuenta en muchos departamentos de Regulatory Affairs y que, en el peor de los casos, puede bloquear la comercialización de una nueva variante de producto.
El escenario
Una familia de productos existente fue introducida legalmente en el mercado antes de la fecha límite y está asignada a una Basic UDI-DI. Para el registro de los productos existentes o de las UDI-DIs existentes, en principio todavía hay tiempo hasta noviembre de 2026.
Ahora, después del 28 de mayo de 2026, se pretende introducir una nueva variante, es decir, una nueva UDI-DI bajo la misma Basic UDI-DI existente.
¿Qué aplica en este caso?
La posición regulatoria clara
Para esta nueva UDI-DI no existe ningún período transitorio adicional.
Las preguntas y respuestas de la Comisión Europea sobre EUDAMED precisan los plazos a nivel de la UDI-DI concreta. Si la primera unidad de un Regulation Device con una UDI-DI específica se introduce en el mercado de la UE en la fecha de uso obligatorio del módulo UDI/Devices o después de dicha fecha, el registro correspondiente en el módulo UDI/DEV debe completarse antes de la primera introducción en el mercado.
Esto significa que una UDI-DI añadida posteriormente no puede apoyarse automáticamente en el período transitorio de la familia de productos existente. Lo decisivo no es únicamente que la familia de productos ya exista, sino cuándo se introduce por primera vez en el mercado la UDI-DI concreta.
El período transitorio hasta noviembre de 2026 aplica a productos o UDI-DIs cuya primera unidad ya fue introducida legalmente en el mercado de la UE antes de la fecha límite y para los cuales se siguen introduciendo en el mercado unidades adicionales de la misma UDI-DI después de dicha fecha.
La consecuencia técnica: La Basic UDI-DI debe estar disponible
Aquí es donde se encuentra el verdadero riesgo práctico.
EUDAMED sigue una estructura clara de tipo padre-hijo: La Basic UDI-DI constituye el nivel superior, bajo el cual se gestionan una o varias UDI-DIs. La Comisión Europea describe expresamente esta estructura: Una o varias UDI-DIs pueden estar vinculadas a una Basic UDI-DI; pueden añadirse UDI-DIs adicionales en una fase posterior. Al mismo tiempo, cada UDI-DI hereda atributos de la Basic UDI-DI vinculada.
En la práctica, esto significa que cualquier fabricante que deba registrar una nueva UDI-DI después del 28 de mayo de 2026 también necesita que la Basic UDI-DI correspondiente esté disponible en el sistema.
En este caso, la Basic UDI-DI debe registrarse de forma anticipada desde una perspectiva técnica y procedimental, aunque las UDI-DIs más antiguas dentro de la misma familia de productos puedan, en teoría, seguir beneficiándose del período transitorio hasta noviembre de 2026.
Esta lógica técnica también está respaldada por las EUDAMED Business Rules: Para una UDI-DI debe existir exactamente una Basic UDI-DI, y varias UDI-DIs pueden asignarse a la misma Basic UDI-DI. Además, una nueva UDI-DI solo puede añadirse a una Basic UDI-DI existente si la Basic UDI-DI tiene el estado “Submitted” o “Registered”.
Riesgo especial con la carga masiva XML y la transmisión M2M
Los fabricantes que transmiten datos UDI mediante carga masiva XML o a través de una interfaz M2M deberían revisar este punto en una fase temprana.
Si un registro de datos referencia una UDI-DI a una Basic UDI-DI que aún no existe en EUDAMED, que no se ha creado correctamente o que todavía no se encuentra en el estado requerido, la transmisión puede fallar durante la validación. La causa raíz no siempre es evidente de inmediato durante el análisis de errores, especialmente cuando se procesan al mismo tiempo varias Basic UDI-DIs, muchas UDI-DIs o estructuras de embalaje complejas.
Esto puede provocar retrasos innecesarios, especialmente en familias de productos grandes, con muchas variantes o con procesos de transmisión automatizados.
Nuestra recomendación práctica
Si se planifica el lanzamiento de un producto con una nueva UDI-DI después del 28 de mayo de 2026, esta nueva variante no debería considerarse de forma aislada.
Se recomienda una revisión estructurada de toda la familia de productos:
- ¿Qué Basic UDI-DI está afectada?
- ¿Qué UDI-DIs existentes ya están asignadas a esta Basic UDI-DI?
- ¿Qué nueva UDI-DI se introducirá después de la fecha límite?
- ¿La Basic UDI-DI ya está disponible en EUDAMED?
- ¿La Basic UDI-DI tiene el estado requerido?
- ¿Se ha preparado correctamente la secuencia técnica de transmisión para XML o M2M?
En muchos casos, es más eficiente preparar y transmitir la familia de productos completa como un conjunto de datos cerrado y validado. Esto reduce la fragmentación, ayuda a evitar errores de referencia y crea claridad regulatoria para cambios posteriores o variantes adicionales.
Nota sobre la base documental
Esta constelación específica —“una nueva UDI-DI bajo una Basic UDI-DI existente después de la fecha límite de EUDAMED”— no se describe como un caso especial independiente en los documentos oficiales.
No obstante, la evaluación se deriva directamente de la combinación de tres fuentes oficiales:
En primer lugar, de las preguntas y respuestas de la Comisión Europea sobre EUDAMED, según las cuales el plazo de registro se considera a nivel de la UDI-DI concreta. Si la primera unidad con una UDI-DI específica se introduce en el mercado en la fecha de uso obligatorio del módulo UDI/Devices o después de dicha fecha, el registro debe completarse antes de la primera introducción en el mercado.
En segundo lugar, de la estructura de EUDAMED entre Basic UDI-DI y UDI-DI, según la cual una o varias UDI-DIs están vinculadas a una Basic UDI-DI y cada UDI-DI hereda atributos de la Basic UDI-DI vinculada.
En tercer lugar, de las EUDAMED Business Rules, según las cuales una UDI-DI debe asignarse exactamente a una Basic UDI-DI y una nueva UDI-DI solo puede añadirse a una Basic UDI-DI existente si la Basic UDI-DI tiene el estado “Submitted” o “Registered”.
Conclusión
Los períodos transitorios de EUDAMED no deberían considerarse únicamente a nivel de la familia de productos. El factor decisivo es cuándo se introduce por primera vez en el mercado la UDI-DI concreta.
Para las nuevas UDI-DIs a partir del 28 de mayo de 2026, la regla es clara: El registro en el módulo EUDAMED UDI/Devices debe completarse antes de la primera introducción en el mercado.
Esto también hace que la Basic UDI-DI correspondiente sea técnicamente relevante. Debe estar disponible y correctamente creada en EUDAMED para el registro de la nueva UDI-DI, incluso si las UDI-DIs más antiguas dentro de la misma familia de productos todavía pueden beneficiarse del período transitorio hasta noviembre de 2026.
Europe IT Consulting apoya a los fabricantes en la preparación estructurada, validación y transmisión de datos UDI a EUDAMED, tanto mediante procesos basados en Excel/XML como a través de interfaces M2M.
Si desea comprobar si sus registros de datos actuales y sus estructuras de carga están preparados para este escenario, póngase en contacto con nosotros.
Ponte en contacto con nosotros
Fuentes
- Comisión Europea: Publicación sobre el uso obligatorio de los cuatro primeros módulos de EUDAMED a partir del 28 de mayo de 2026.
https://health.ec.europa.eu/latest-updates/eudamed-four-first-modules-will-be-mandatory-use-28-may-2026-2025-11-27_en - Comisión Europea: EUDAMED Overview – uso obligatorio de los cuatro primeros módulos, incluidos Actor Registration y UDI/Device Registration.
https://health.ec.europa.eu/medical-devices-eudamed/overview_en - Comisión Europea: UDI/Device Registration – presentación de información UDI/device en EUDAMED.
https://health.ec.europa.eu/medical-devices-eudamed/udidevice-registration_en - Comisión Europea: Q&A on the gradual roll-out of EUDAMED – plazos para el módulo UDI/DEV a nivel de UDI-DI.
https://health.ec.europa.eu/document/download/0e7327c7-0e06-4fbd-90d3-8ab7bb30fe9f_en?filename=md_eudamed-qa_en.pdf - Comisión Europea: EUDAMED UDI Concept – estructura de Basic UDI-DI, UDI-DI y Package UDI-DI.
https://health.ec.europa.eu/system/files/2021-11/md_eudamed-udi-concept_en_0.pdf - Comisión Europea: EUDAMED UDI/Device Business Rules – asignación de UDI-DI a Basic UDI-DI y adición de nuevas UDI-DIs.
https://health.ec.europa.eu/system/files/2022-08/md_udi-device-business-rules_en_0.pdf







Related Posts