La solución inteligente para una gestión conforme de datos UDI en swissdamed
Preparación estructurada de su registro de productos en swissdamed: eficiente, trazable y conforme con los requisitos regulatorios.
Su desafío es nuestra solución
Con swissdamed, Swissmedic opera la base de datos central suiza para productos sanitarios, productos sanitarios de diagnóstico in vitro, así como sistemas y packs de procedimiento. Para fabricantes, Representantes Autorizados Suizos y otros operadores económicos, esto supone un nuevo reto operativo: los datos UDI deben prepararse, comprobarse y presentarse de forma completa, estructurada y conforme a los requisitos de swissdamed.
Nuestra plantilla Excel para swissdamed ofrece el primer paso estructurado: desarrollada por expertos en UDI para empresas que desean preparar sus datos de producto de manera eficiente, transparente y con un claro enfoque en el cumplimiento regulatorio.
Por favor, complete el formulario para solicitar una oferta
La plantilla Excel UDI para swissdamed de un vistazo:
Pestañas completas para sus datos UDI relevantes para swissdamed:
- Pestaña Basic UDI-DI:
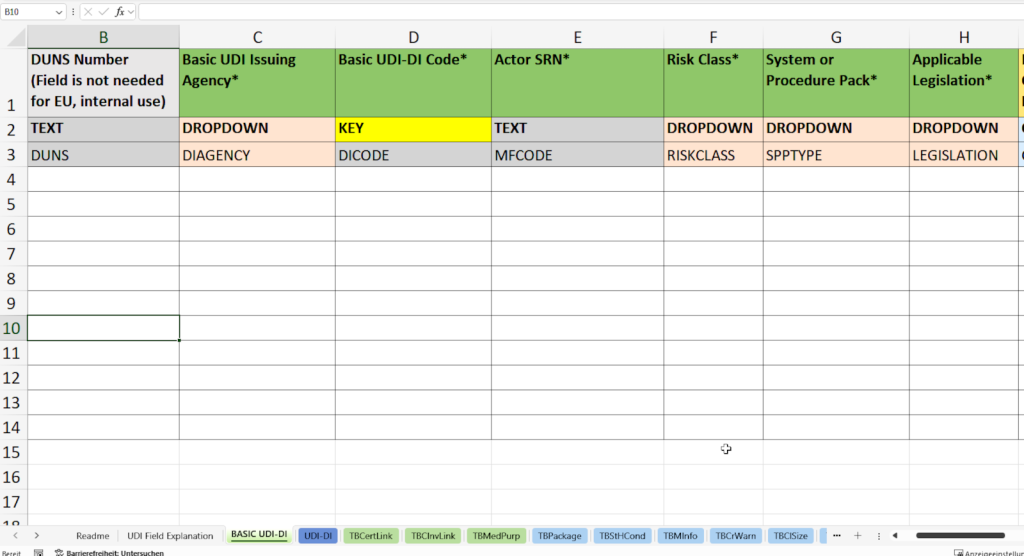 En esta pestaña se registran los datos maestros superiores para la identificación única de su familia de productos. Estos datos constituyen la base para la asignación estructurada de los UDI-DI individuales en el módulo UDI Devices de swissdamed.
En esta pestaña se registran los datos maestros superiores para la identificación única de su familia de productos. Estos datos constituyen la base para la asignación estructurada de los UDI-DI individuales en el módulo UDI Devices de swissdamed.
- Asignación y documentación del Basic UDI-DI conforme a las especificaciones de la entidad emisora responsable, por ejemplo GS1, HIBCC o ICCBBA.
- Asignación del operador económico responsable, por ejemplo fabricante suizo, Representante Autorizado Suizo o fabricante de sistemas y packs de procedimiento.
- Registro de información relevante del actor, en particular el CHRN o la información del actor registrada en swissdamed.
- Asignación del tipo de producto y la clase de riesgo conforme a los requisitos aplicables de MedDO/IvDO o las estructuras subyacentes MDR/IVDR.
- Definición de si el producto es un producto sanitario, un diagnóstico in vitro, un sistema o un pack de procedimiento.
- Documentación de características como dispositivo activo, función de medición, función de administración, dispositivo implantable, instrumento quirúrgico reutilizable u otros tipos especiales de producto.
- Registro del modelo del producto, nombre del producto y otra información descriptiva relacionada con la familia de productos.
- Especificación de componentes o características especiales, por ejemplo tejidos o células de origen animal o humano, sustancias CMR/endocrinas u otra información relevante desde el punto de vista regulatorio.
Por favor, complete el formulario para solicitar una oferta
- Pestaña UDI-DI:
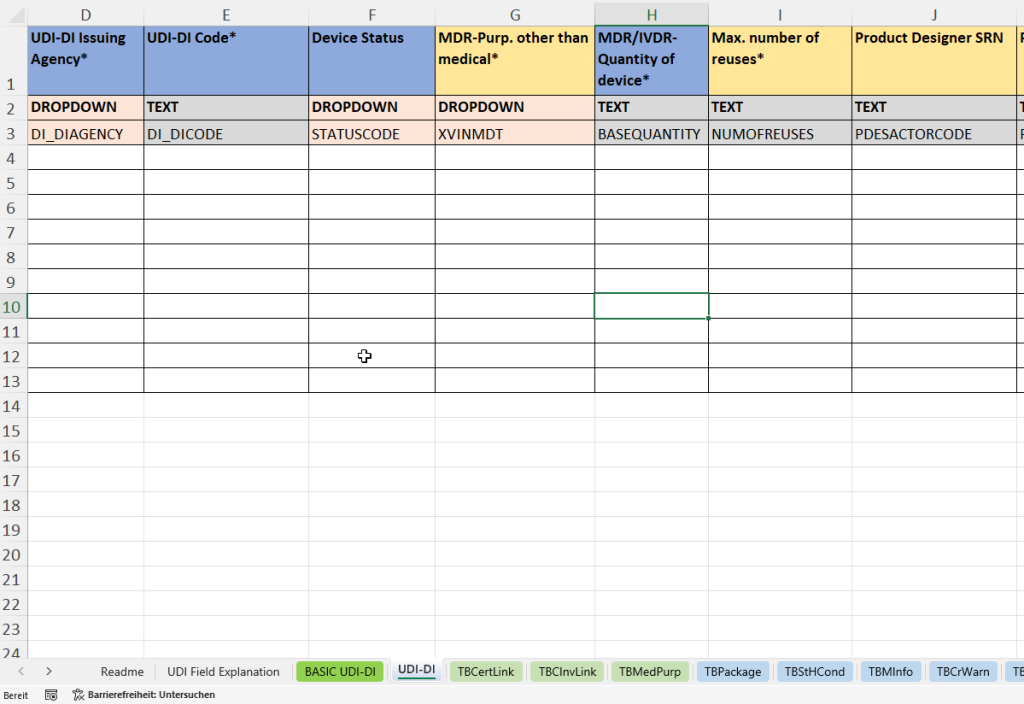 En esta pestaña se registran todos los datos individuales específicos del producto necesarios para la identificación única y la trazabilidad de un producto sanitario o IVD concreto. El UDI-DI sirve como identificador central para el registro del producto en swissdamed.
En esta pestaña se registran todos los datos individuales específicos del producto necesarios para la identificación única y la trazabilidad de un producto sanitario o IVD concreto. El UDI-DI sirve como identificador central para el registro del producto en swissdamed.
- Vinculación con el Basic UDI-DI superior para la asignación a una familia de productos.
- Registro del número de material interno y de la descripción del material para una asignación inequívoca dentro de su empresa.
- Asignación del UDI-DI por una entidad emisora reconocida e introducción del código UDI-DI único.
- Definición del estado del producto, por ejemplo activo, inactivo, retirado o en preparación.
- Registro de la cantidad por unidad de venta, así como información adicional sobre la lógica del producto y del embalaje.
- Documentación del número de referencia para la identificación en la documentación técnica, el etiquetado o el embalaje.
- Información sobre el marcado directo en el producto, cuando sea relevante.
- Etiquetado estéril e indicación de si se requiere esterilización antes del uso.
- Indicación de si el producto está etiquetado como de un solo uso o si ha sido reprocesado.
- Identificación de producción: número de lote o partida, fecha de caducidad, fecha de fabricación, número de serie y versión de software.
- Identificadores adicionales como Secondary UDI-DI, Unit of Use DI u otros identificadores, cuando sean necesarios.
- Información adicional, como URL para instrucciones electrónicas de uso u otra información del producto.
- Información del certificado:
- Registro del código Basic UDI-DI relacionado para una vinculación clara con el certificado.
- Introducción del número de certificado y gestión del número de revisión, por ejemplo en caso de renovaciones o modificaciones.
- Selección del tipo de certificado e indicación del organismo notificado, cuando sea relevante para el producto.
- Documentación de la fecha de expiración y otros datos del certificado para productos en los que esta información sea necesaria para el registro.
- Investigación clínica / estudio de rendimiento
- Introducción de identificadores relevantes para investigaciones clínicas o estudios de rendimiento, cuando deban especificarse para el producto.
- Indicación del país en el que se realizó la investigación clínica o el estudio de rendimiento.
- Idioma y finalidad médica
- Selección del idioma en el que se proporciona la información relacionada con el producto.
- Descripción de la finalidad médica, así como otra información del producto dependiente del idioma.
- Información de embalaje / jerarquía de embalaje:
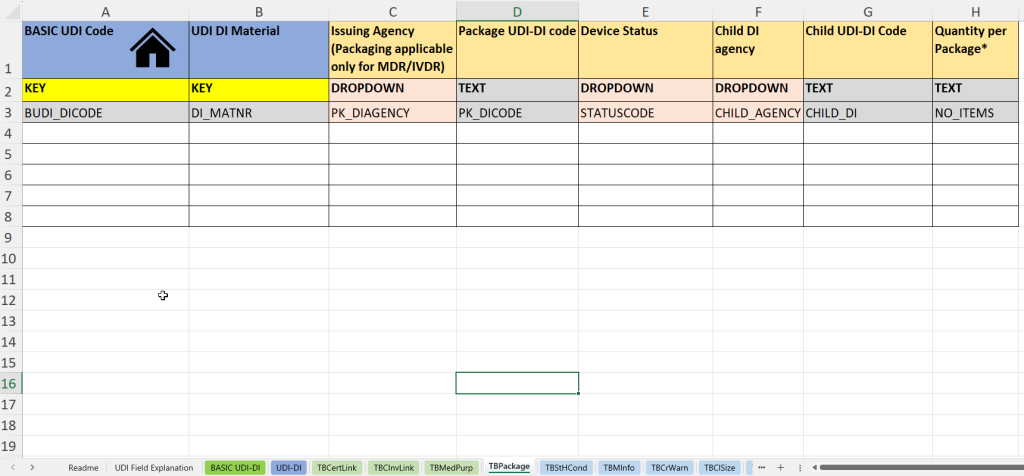 En esta pestaña se documenta la información sobre unidades de embalaje y estructuras UDI-DI subordinadas, especialmente relevante para embalajes multinivel, sets, así como sistemas y packs de procedimiento.
En esta pestaña se documenta la información sobre unidades de embalaje y estructuras UDI-DI subordinadas, especialmente relevante para embalajes multinivel, sets, así como sistemas y packs de procedimiento.
- Número de material interno de la unidad de embalaje para una identificación inequívoca.
- Entidad emisora para el UDI-DI del embalaje.
- Introducción del código UDI-DI del embalaje, por ejemplo para embalaje exterior, sets o jerarquías de embalaje multinivel.
- Estado de la unidad de embalaje.
- Especificación de UDI-DI subordinados dentro de la unidad de embalaje.
- Cantidad por embalaje para la correcta representación de la jerarquía de embalaje.
- Condiciones de almacenamiento y manipulación
- Asignación de condiciones de almacenamiento y manipulación al UDI-DI correspondiente.
- Especificación del tipo de condición, por ejemplo temperatura, humedad, protección frente a la luz u otros requisitos.
- Descripción dependiente del idioma para explicar con mayor detalle instrucciones específicas de almacenamiento o manipulación.
Por favor, complete el formulario para solicitar una oferta
- Advertencias críticas
- Selección y documentación de tipos de advertencia relevantes, por ejemplo implante, látex, radioactividad u otras advertencias relacionadas con el producto.
- Información sobre tamaños
- Especificación del formato del tamaño, por ejemplo numérico, alfanumérico o simbólico.
- Exactitud o precisión de la información sobre el tamaño.
- Unidad de tamaño, así como valores mínimos y máximos.
- Sustancias médicas humanas
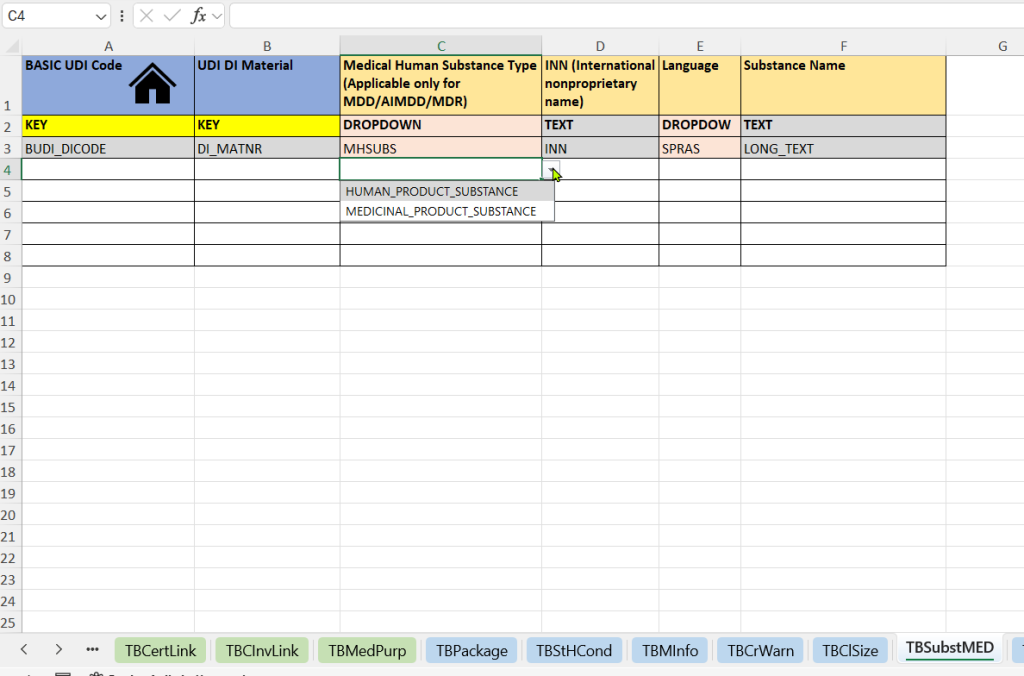
- Selección del tipo de sustancia.
- Introducción del nombre común internacional, cuando esté disponible.
- Indicación del idioma para la representación específica por idioma.
- Denominación en texto libre de la sustancia, por ejemplo nombre nacional comúnmente utilizado o descripción adicional.
- Sustancias CMR/endocrinas
- Selección del tipo de sustancia, por ejemplo categoría CMR o disruptor endocrino.
- Especificación del código CAS y del código EC, cuando estén disponibles.
- Nombre o descripción de la sustancia dependiente del idioma.
- Descripción adicional del producto
- Selección del idioma en el que debe proporcionarse la descripción adicional.
- Registro de información complementaria del producto, por ejemplo sobre función, composición, características específicas del set o variante específica del producto.
- Nombre comercial
- Selección del idioma para el nombre comercial.
- Introducción del nombre comercial, por ejemplo nombre del producto, nombre del modelo o denominación relevante para el mercado.
- Código de nomenclatura
- Selección y documentación del código de nomenclatura adecuado conforme a los requisitos relevantes para swissdamed.
Por favor, complete el formulario para solicitar una oferta
Funciones inteligentes para la máxima eficiencia:
- Resaltado en color de campos obligatorios:

- Identificación visual inmediata de entradas obligatorias.
- Diferenciación entre campos absolutamente obligatorios y campos requeridos de forma condicional.
- Visualización contextual de campos relevantes en función de entradas anteriores.
- Menús desplegables validados:
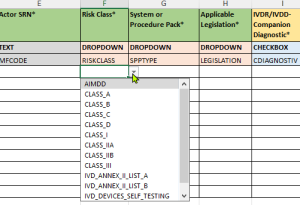
- Opciones de selección predefinidas conforme a las estructuras de datos relevantes para swissdamed.
- Reducción de errores de entrada mediante opciones estandarizadas.
- Terminología coherente para Regulatory Affairs, Quality Management e IT.
- Comprobaciones automáticas de dependencias:
- Ajuste dinámico de los campos de entrada en función del tipo de producto, la clasificación y el rol del actor.
- Comprobación lógica de la coherencia de los datos entre diferentes pestañas.
- Advertencias en caso de posibles incoherencias en la entrada de datos.
- Soporte bilingüe:
- Descripciones paralelas en alemán e inglés.
- Uso internacional para equipos globales, Representantes Autorizados Suizos y socios externos.
- Terminología coherente para swissdamed, datos UDI y procesos regulatorios.
- Soporte documental:
- Explicaciones integradas para campos complejos.
- Notas sobre requisitos regulatorios y dependencias de datos.
- Apoyo en la preparación de datos para revisión, conversión y presentación.
Oferta integral de servicios para su cumplimiento con swissdamed
- Plantilla Excel UDI para swissdamed: la base profesional para la entrada estructurada de datos UDI y la preparación del registro de productos en swissdamed.
- Revisión y validación de datos: Le apoyamos en la revisión especializada de sus datos UDI para que las inconsistencias típicas puedan identificarse y corregirse antes de la presentación.
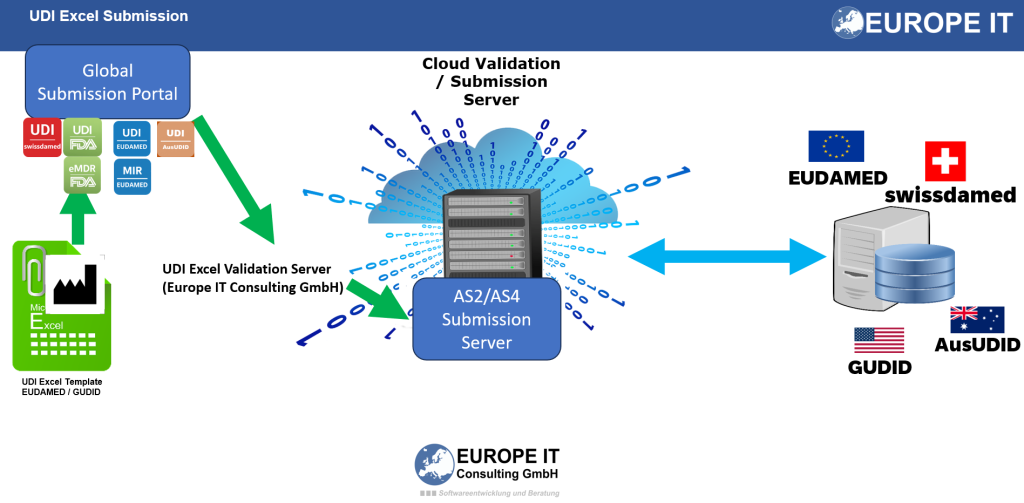
- Preparación XML y de carga: La conversión de sus datos estructurados a un formato técnico adecuado es proporcionada como servicio separado por nuestros expertos.
- Servicio de presentación en swissdamed: Acompañamos todo el proceso de presentación de datos: desde la preparación y las pruebas en Playground hasta el registro productivo, tan pronto como las funciones correspondientes estén disponibles y sean aplicables.
Especificaciones técnicas de la plantilla Excel
- Formato de archivo: Microsoft Excel (.xlsx)
- Compatibilidad: Microsoft Excel 2016 y versiones posteriores
- Tamaño: Optimizada para tiempos de carga rápidos, incluso con conjuntos de datos extensos
- Seguridad: Estructuras protegidas por contraseña para evitar cambios no deseados
- Actualizaciones: Actualizaciones periódicas conforme a nuevos requisitos de swissdamed y especificaciones técnicas
- Validación de datos: Rutinas de comprobación integradas para entradas coherentes
Por favor, complete el formulario para solicitar una oferta
Por qué las empresas líderes de tecnología médica confían en nuestra solución
Europe IT Consulting GmbH no solo cuenta con certificación ISO 9001 y es partner de SAP: somos su socio estratégico para la transformación digital de sus procesos regulatorios. Nuestro enfoque se centra en la gestión de datos UDI, la validación de datos y la preparación técnica de presentaciones regulatorias.
Lo que hace única a nuestra plantilla Excel para swissdamed:
- Estructuración precisa conforme a los requisitos del módulo UDI Devices de swissdamed
- Menús desplegables inteligentes con opciones de selección validadas
- Resaltado visual de campos obligatorios y campos dependientes
- Navegación intuitiva por el complejo mundo de los datos UDI
- Soporte multilingüe para equipos internacionales, Representantes Autorizados Suizos y socios externos
- Preparación óptima para revisión de datos, conversión técnica y presentación en swissdamed
- ANALIZAR: Identifique la necesidad de acción para su registro de productos en swissdamed. «El primer paso hacia un cumplimiento UDI suizo estructurado»
- ADQUIRIR: Asegure el acceso a nuestra plantilla Excel para swissdamed. «La base de su estrategia de datos regulatorios para Suiza»
- IMPLEMENTAR: Registre sus datos de producto en una estructura de plantilla clara y revisable. «No más entradas de datos UDI poco claras»
- BENEFICIARSE: Encárguenos la validación, la preparación técnica y la presentación en swissdamed. «Concéntrese en su actividad principal mientras nosotros le apoyamos en la implementación técnica»
Perfectamente alineada con sus requisitos individuales
Para carteras de productos pequeñas y medianas:
La plantilla Excel es la base ideal para una entrada de datos estructurada, complementada por nuestro servicio de revisión, conversión y presentación.
Para líneas de productos extensas:
La base perfecta para procesos escalables de carga o M2M para volúmenes de datos mayores, con apoyo adicional de nuestros expertos en IT y UDI.
Para usuarios de SAP:
Maximice su beneficio mediante una integración fluida con nuestras soluciones UDI y los datos maestros regulatorios existentes.
Para empresas con datos EUDAMED existentes:
Utilice los conjuntos de datos existentes como punto de partida; sin embargo, swissdamed es una base de datos suiza independiente. No existe sincronización automática con EUDAMED. Los datos deben prepararse y presentarse activamente para swissdamed.
Preguntas frecuentes para apoyar su decisión
¿Existen costes adicionales por actualizaciones de la plantilla Excel?
Las actualizaciones importantes de la plantilla están incluidas en la compra, siempre que se refieran al mantenimiento regular de la estructura de la plantilla y de las listas de valores. En caso de cambios regulatorios o técnicos extensos, puede ser necesaria una coordinación separada.
¿Puedo utilizar la plantilla Excel para crear archivos XML para swissdamed por mi cuenta?
No. La plantilla Excel sirve principalmente para el registro estructurado y la preparación de sus datos UDI. La conversión técnica o la preparación para la carga se ofrece por nuestra parte como servicio separado.
¿Cómo se presentan mis datos en swissdamed?
Después de la entrada de datos, puede utilizar nuestro servicio de presentación. Dependiendo del estado del proyecto y de la disponibilidad de funciones técnicas, le apoyamos con la presentación manual, la preparación XML, las pruebas en Playground y la preparación M2M.
¿Puedo utilizar datos EUDAMED existentes para swissdamed?
Sí, los datos EUDAMED existentes pueden servir a menudo como un valioso punto de partida. No obstante, los datos deben comprobarse, adaptarse y presentarse activamente para swissdamed. No existe sincronización automática entre EUDAMED y swissdamed.
¿Qué requisitos previos necesito para swissdamed?
Por regla general, el operador económico responsable debe estar registrado en swissdamed. Dependiendo del rol, esto puede aplicarse, por ejemplo, a fabricantes suizos, Representantes Autorizados Suizos o fabricantes de sistemas y packs de procedimiento. Para determinados procesos, se requieren derechos de usuario, roles y credenciales técnicas de acceso adicionales.
¿Cómo se protegen los datos introducidos?
La plantilla Excel almacena los datos localmente en su archivo. Además, recomendamos realizar copias de seguridad periódicas conforme a sus requisitos internos de IT y gestión de calidad.
¿Puedo utilizar la plantilla para varios productos o líneas de productos?
Sí. La plantilla está diseñada para gestionar varios Basic UDI-DI y numerosos UDI-DI asociados en un formato estructurado.
¿Necesito conocimientos especiales de Excel?
No. Los conocimientos básicos de Excel son suficientes. La estructura, los menús desplegables, los indicadores de color y las explicaciones apoyan a los usuarios durante la entrada de datos.
¿Se actualizará la plantilla en caso de cambios regulatorios?
Sí. Supervisamos los desarrollos relevantes de swissdamed y adaptamos la plantilla cuando cambian las estructuras de datos, las listas de valores o los requisitos técnicos.
Actúe ahora: asegure su ventaja para el registro de productos en Suiza.
Las obligaciones de registro en swissdamed se acercan. Las empresas que estructuran, validan y preparan técnicamente sus datos UDI en una fase temprana reducen riesgos posteriores, ciclos de corrección y cuellos de botella operativos.
Su primer paso hacia un cumplimiento eficiente con swissdamed:
Por favor, complete el formulario para solicitar una oferta
Invierta ahora en una estrategia estructurada de datos regulatorios para Suiza.
La plantilla Excel UDI para swissdamed es desarrollada y distribuida por Europe IT Consulting GmbH, su socio certificado para soluciones informáticas regulatorias desde 2011.