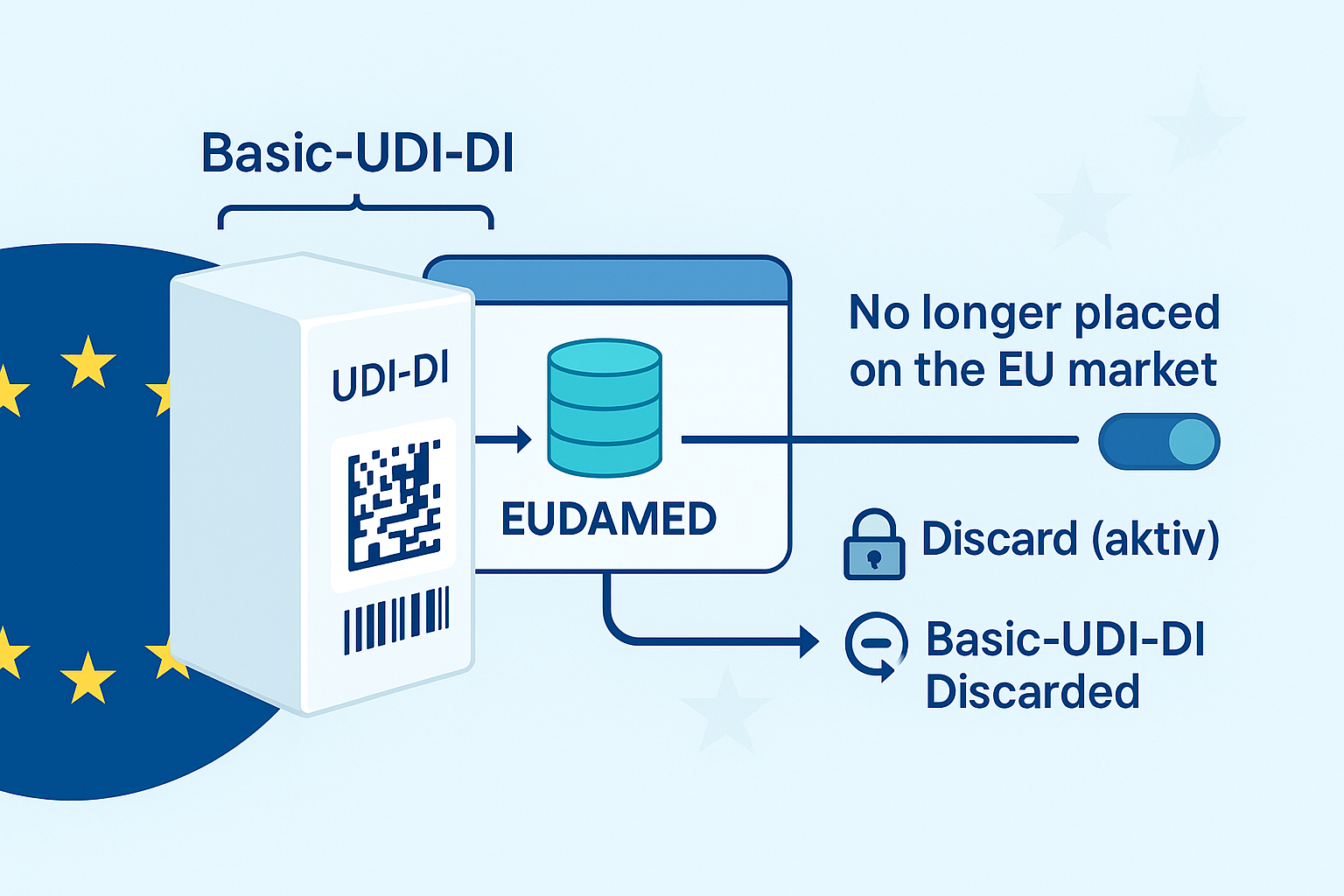
Basic-UDI-DI in Übergangsszenarien: Darf eine BUDI „leer“ sein?
1. Kann eine Basic-UDI-DI (übergangsweise) ohne zugehörige UDI-DI(s) bestehen?
Nein – in EUDAMED wird eine Basic-UDI-DI nicht isoliert registriert. Bei der Registrierung von Regulation Devices verlangt der offizielle EUDAMED-User-Guide, dass eine Basic-UDI-DI immer zusammen mit mindestens einer UDI-DI eingereicht wird („…you cannot register a Basic UDI without a UDI-DI“). European Comission- UDI Devices User Guide
2. Was passiert mit der Basic-UDI-DI, wenn die letzte zugehörige UDI-DI auf „No longer placed on the EU market“ gesetzt wird?
Der Statuswechsel löscht weder die UDI-DI noch die Basic-UDI-DI. Laut User-Guide blendet der Status „No longer placed on the EU market“ die Market-Information aus; verknüpfte Container-Packages werden automatisch auf denselben Status gesetzt. Eine Löschung erfolgt nicht automatisch, sondern ausschließlich per „Discard“ (bewusste Aktion). European Comission- UDI Devices User Guide
Falls man allerdings die letzte UDI-DI aktiv „discardet“, gilt laut offiziellen Business Rules: Dann wird auch die zugehörige Basic-UDI-DI auf „Discarded“ gesetzt (logisches Delete); „Discarded“-Einträge sind nicht mehr öffentlich sichtbar und Codes können wiederverwendet werden. Zudem ist „Discard“ gesperrt, wenn die Basic-UDI-DI z. B. in Zertifikaten referenziert ist oder das Gerät in Vigilanzmeldungen vorkommt. Europäische Kommission-Business Rules
3. Was, wenn das Produkt gar nicht in EUDAMED angemeldet würde, jedoch intern bereits eine BUDI besteht?
-
EUDAMED-seitig existiert dann kein Datensatz – da eine Basic-UDI-DI nicht ohne UDI-DI registriert werden kann (siehe 1).
-
Rechtlich (MDR): Vor dem Inverkehrbringen muss der Hersteller der UDI-Datenbank die Basic-UDI-DI samt Kerndaten übermitteln; die Basic-UDI-DI ist Hauptschlüssel in der UDI-Datenbank und wird in Zertifikaten und in der EU-Konformitätserklärung genannt (Annex VI/IV). EUR-Lex+1
-
Zur aktuellen Pflicht zur EUDAMED-Nutzung: Die Nutzung des UDI/Device-Moduls ist derzeit (Stand heute) laut EU-Kommission noch nicht verbindlich; Einträge sind freiwillig, bis die jeweiligen Module per Amtsblatt-Mitteilung verpflichtend werden (phasenweise Roll-out; neue Rechtslage 2024/1860). Nationale Zusatzpflichten sind möglich.




Related Posts