Die smarte Lösung für strukturierte AusUDID UDI-Datenverwaltung
Bereiten Sie Ihre UDI-Daten für die Australian UDI Database strukturiert, prüfbar und effizient vor.
Ihr Problem ist unsere Lösung
Mit der Australian Unique Device Identification Database, kurz AusUDID, führt die Therapeutic Goods Administration (TGA) eine zentrale UDI-Datenbank für Medizinprodukte und In-vitro-Diagnostika ein, die in Australien bereitgestellt werden. Für Hersteller, Sponsoren und weitere beteiligte Organisationen entsteht dadurch eine neue operative Herausforderung: UDI-Daten müssen vollständig, konsistent und entsprechend den Anforderungen der TGA vorbereitet, geprüft und eingereicht werden.
Unsere AusUDID Excel-Vorlage bietet Ihnen den ersten strukturierten Schritt – entwickelt von UDI-Experten für Unternehmen, die ihre australischen UDI-Daten effizient vorbereiten und spätere Validierungsfehler vermeiden möchten.
Bitte füllen Sie das Formular aus für ein Angebot
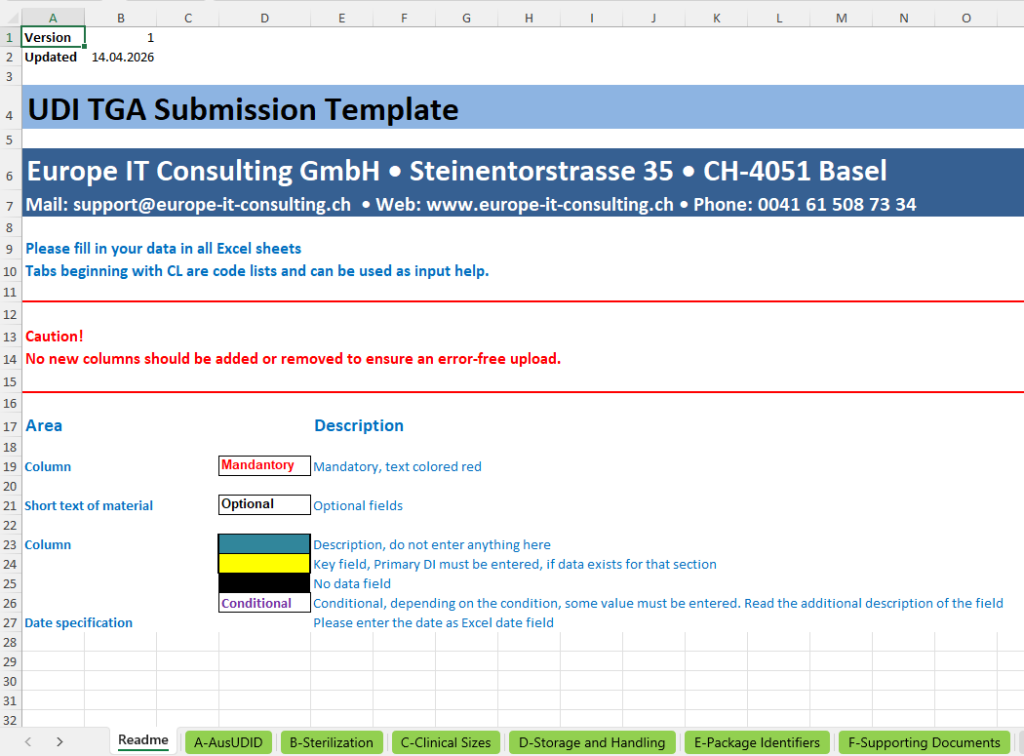
Die AusUDID UDI Excel-Vorlage auf einen Blick:
Die Vorlage ist in fachliche Eingaberegister und technische Code-Listen gegliedert.
Die eigentliche Datenerfassung erfolgt in den Registern A bis F. Die Register mit dem Präfix „CL_“ enthalten Code-Listen und Auswahlwerte, die als Eingabehilfe und Validierungsgrundlage dienen. Dadurch wird sichergestellt, dass die Dateneingabe nicht frei und unkontrolliert erfolgt, sondern anhand vordefinierter Werte und regulatorisch relevanter Auswahllogik.
A-AusUDID – Zentrales Hauptregister für den UDI-Datensatz
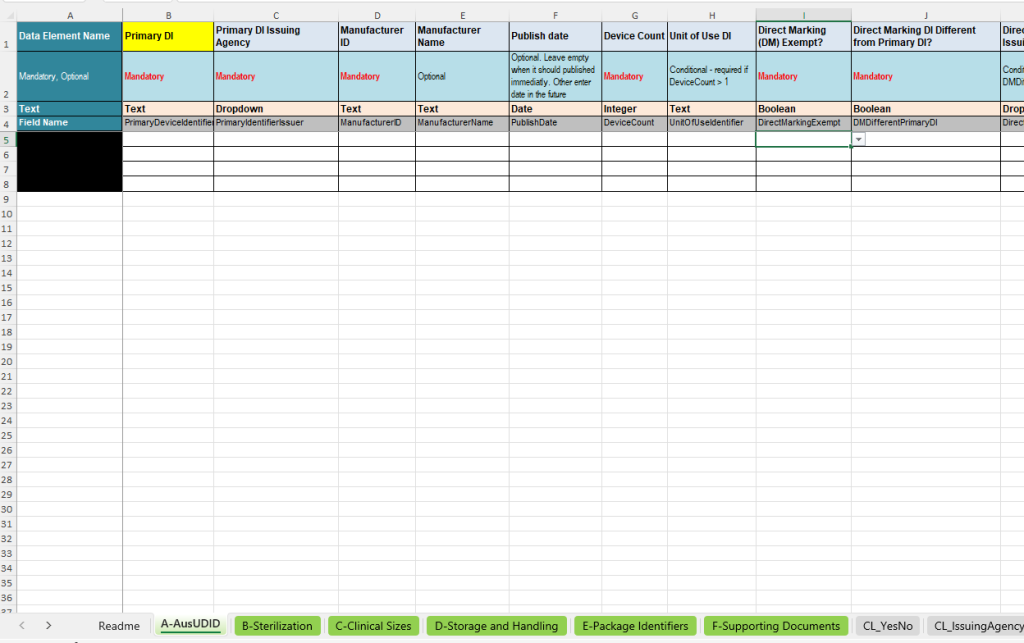
Das Register A-AusUDID ist das zentrale Hauptregister der Vorlage. Hier werden die wichtigsten Stammdaten eines UDI-Datensatzes gepflegt. Der Primary Device Identifier bildet dabei den zentralen Schlüssel, über den die weiteren Zusatzregister mit dem jeweiligen Produkt verknüpft werden.
- Primary Device Identifier: Zentrale Gerätekennung für die eindeutige Identifikation des Produkts.
- Primary DI Issuing Agency: Angabe der Vergabestelle, z. B. GS1, HIBCC oder ICCBBA.
- Manufacturer ID und Manufacturer Name: Identifikation und Name des Herstellers.
- Publish Date: Optionales Veröffentlichungsdatum, falls der Datensatz nicht sofort veröffentlicht werden soll.
- Device Count und Unit of Use DI: Erfassung der Anzahl der enthaltenen Produkte und, falls erforderlich, der Unit-of-Use-Kennung.
- Direct Marking: Angaben dazu, ob eine direkte Markierung erforderlich ist, ob eine Ausnahme vorliegt und ob eine abweichende Direct Marking DI verwendet wird.
- Brand Name und Model/Version: Produktname, Modell oder Versionsbezeichnung.
- Device Class: Auswahl der australischen Risikoklasse, z. B. Class III, Class IIb, Class IIa, Class I oder IVD-Klassen.
- Software- und Kit-Informationen: Angabe, ob es sich um Software, Software as a Medical Device oder ein Kit handelt.
- Device Description und GMDN Code: Beschreibung des Produkts und Zuordnung zur Global Medical Device Nomenclature.
- ARTG ID, Catalogue Number und Sponsor Commercial Distribution End Date: Angaben zur Verknüpfung mit dem Australian Register of Therapeutic Goods sowie sponsorbezogene Vertriebsinformationen.
- MRI Safety Status: Klassifizierung der MRT-Sicherheit, z. B. MR Safe, MR Conditional oder MR Unsafe.
- Single Use und Reuse: Angaben zur Einmalverwendung und gegebenenfalls zur begrenzten Wiederverwendbarkeit.
- Latex- und Naturkautschuk-Kennzeichnung: Erfassung relevanter Labeling-Angaben zu Latex oder natürlichem Kautschuk.
- Sterilität und Sterilisation: Angaben dazu, ob das Produkt steril verpackt ist oder vor Gebrauch sterilisiert werden muss.
- Production Identifier: Kennzeichnung, ob Lot/Batch, Herstellungsdatum, Seriennummer, Ablaufdatum oder Donation ID Number auf dem Label vorhanden sind.
- Secondary DI und Previous DI: Dokumentation zusätzlicher oder vorheriger Gerätekennungen inklusive jeweiliger Vergabestelle.
Nutzen: Dieses Hauptregister schafft die zentrale Datenbasis für die AusUDID-Einreichung. Es bündelt alle wesentlichen Produkt-, Hersteller-, Labeling-, Klassifizierungs- und Identifikationsinformationen in einer strukturierten Tabelle.
Bitte füllen Sie das Formular aus für ein Angebot
B-Sterilization – Sterilisationsmethoden
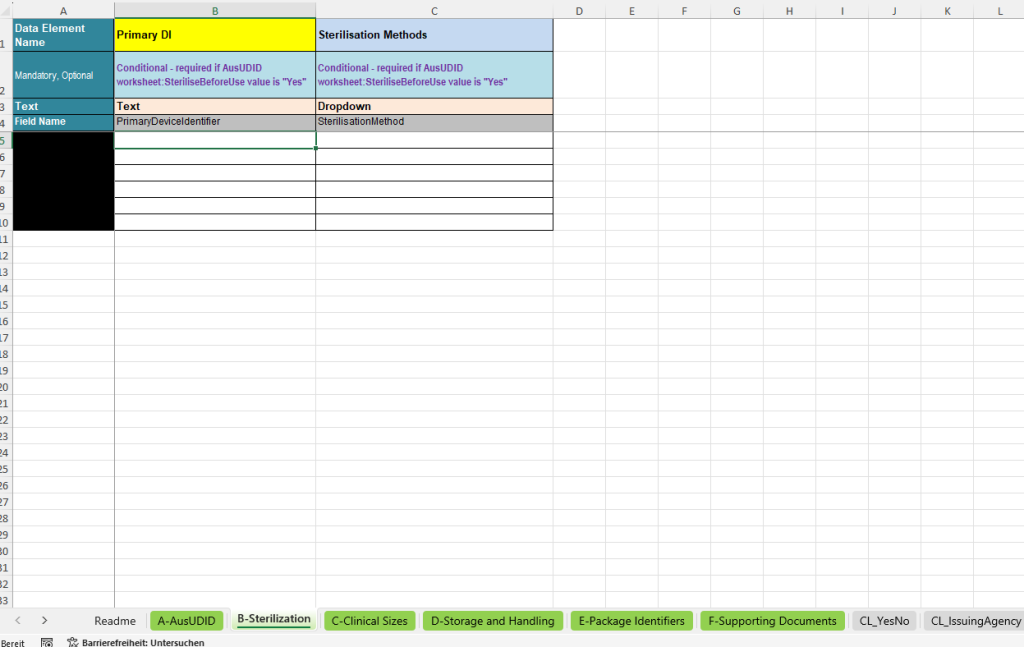
Das Register B-Sterilization wird verwendet, wenn im Hauptregister angegeben wurde, dass das Produkt vor Gebrauch sterilisiert werden muss. In diesem Fall müssen die relevanten Sterilisationsmethoden strukturiert zum jeweiligen Primary Device Identifier erfasst werden.
- Primary DI: Verknüpfung mit dem entsprechenden UDI-Datensatz aus dem Hauptregister.
- Sterilisation Methods: Auswahl der zutreffenden Sterilisationsmethode über eine definierte Auswahlliste.
Die Vorlage unterstützt unterschiedliche Sterilisationsmethoden wie z. B. Ethylenoxid, Dampfsterilisation, trockene Hitze, Gamma-Strahlung, Elektronenstrahl, Wasserstoffperoxid, Plasma oder weitere Verfahren.
Nutzen: Sterilisationsinformationen werden nicht unstrukturiert im Hauptregister gepflegt, sondern in einem eigenen Register geführt. Dadurch können mehrere relevante Methoden sauber zum jeweiligen Produkt zugeordnet werden.
C-Clinical Sizes – Klinische Größenangaben
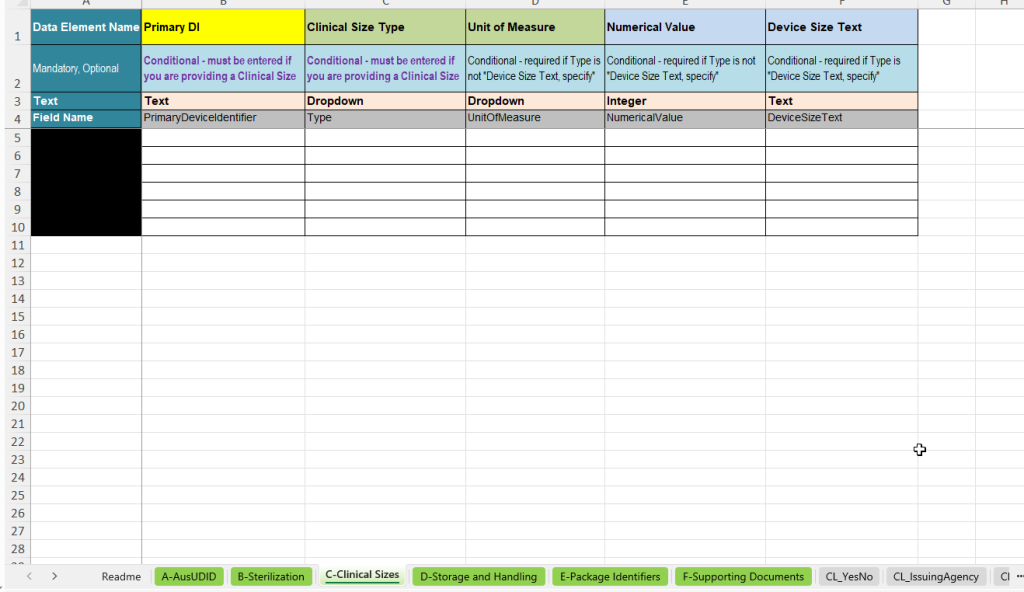
Das Register C-Clinical Sizes dient zur Erfassung klinisch relevanter Größeninformationen. Es wird verwendet, wenn Produktgröße, Dimension oder andere relevante Größenmerkmale für die AusUDID-Datenmeldung angegeben werden sollen oder müssen.
- Primary DI: Verknüpfung mit dem entsprechenden UDI-Datensatz.
- Clinical Size Type: Auswahl der Art der Größenangabe, z. B. Länge, Fläche, Winkel, Gauge oder andere Größenkategorien.
- Unit of Measure: Einheit der Größenangabe, z. B. Millimeter, Zentimeter, Inch, Degree oder andere Einheiten.
- Numerical Value: Numerischer Wert der Größenangabe.
- Device Size Text: Freitextfeld, wenn die Größe nicht sinnvoll numerisch abgebildet werden kann oder als spezifischer Text angegeben werden soll.
Die Vorlage unterscheidet zwischen numerischen Größenangaben und reinen Textgrößen. Wenn eine standardisierte Größe mit Einheit angegeben wird, werden Typ, Einheit und Wert gepflegt. Wenn die Größe nur als Text sinnvoll darstellbar ist, wird das Feld Device Size Text verwendet.
Nutzen: Klinische Größen werden konsistent und auswertbar erfasst. Gleichzeitig bleibt die Vorlage flexibel genug für Produkte, deren Größenangaben nicht rein numerisch dargestellt werden können.
D-Storage and Handling – Lagerungs- und Handhabungsbedingungen
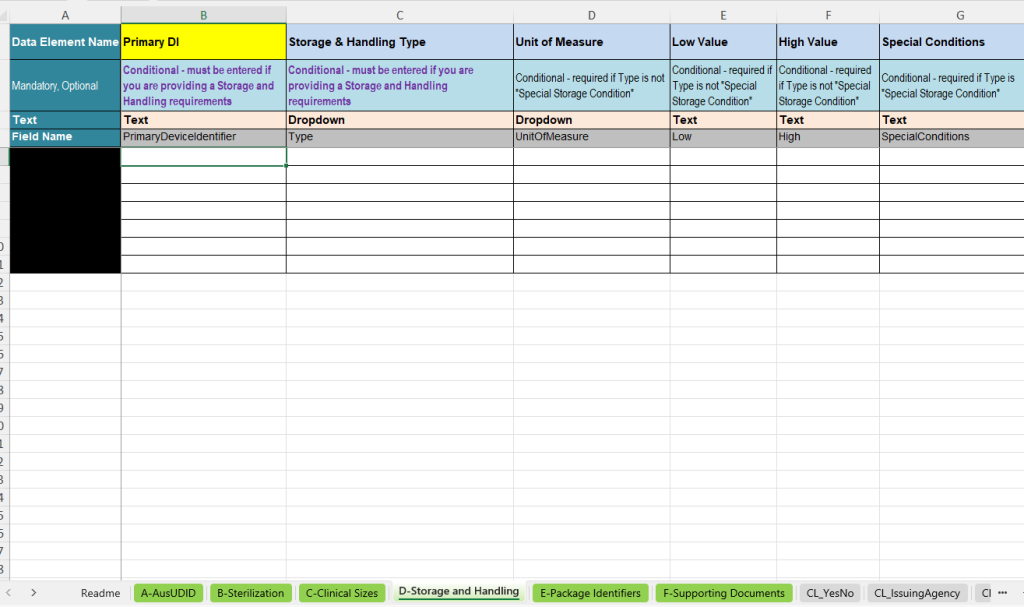
Das Register D-Storage and Handling dokumentiert besondere Lagerungs- und Handhabungsanforderungen des Produkts. Diese Informationen sind wichtig, wenn bestimmte Umweltbedingungen oder besondere Hinweise für Lagerung und Transport einzuhalten sind.
- Primary DI: Zuordnung der Bedingung zum jeweiligen UDI-Datensatz.
- Storage & Handling Type: Auswahl der Art der Bedingung, z. B. Temperatur, Luftfeuchtigkeit, atmosphärischer Druck oder spezielle Lagerbedingung.
- Unit of Measure: Einheit für die jeweilige Bedingung, z. B. Grad Celsius, Fahrenheit, Kelvin, Prozent relative Luftfeuchtigkeit, kPa oder mbar.
- Low Value und High Value: Unterer und oberer Grenzwert für die entsprechende Bedingung.
- Special Conditions: Freitextfeld für besondere Bedingungen, wenn keine numerischen Grenzwerte verwendet werden.
Die Vorlage enthält eine Logik, bei der numerische Grenzwerte und Einheit verwendet werden, wenn es sich um messbare Bedingungen handelt. Bei speziellen Lagerbedingungen kann stattdessen eine textliche Beschreibung gepflegt werden.
Nutzen: Kritische Lagerungs- und Handhabungsdaten werden strukturiert erfasst und können produktbezogen geprüft werden. Dadurch lassen sich unklare Freitextangaben und widersprüchliche Grenzwerte vermeiden.
Bitte füllen Sie das Formular aus für ein Angebot
E-Package Identifiers – Verpackungskennungen und Verpackungshierarchie
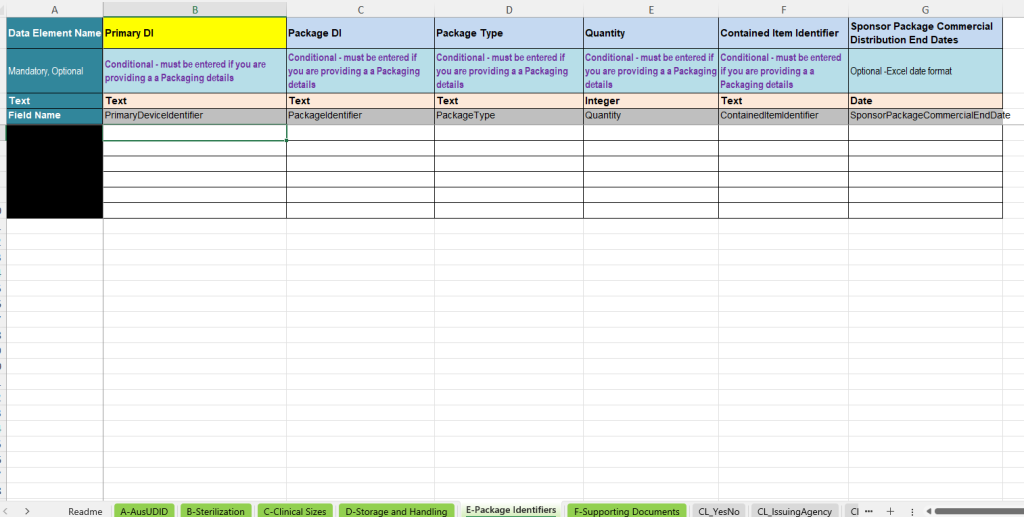
Das Register E-Package Identifiers dient zur Erfassung zusätzlicher Verpackungskennungen und Verpackungsinformationen. Es ist insbesondere relevant, wenn neben dem Primary Device Identifier weitere Verpackungsebenen oder enthaltene Einheiten dokumentiert werden müssen.
- Primary DI: Verknüpfung mit dem Hauptdatensatz.
- Package DI: Kennung der Verpackungseinheit.
- Package Type: Art der Verpackungseinheit, z. B. Verpackungsebene oder Verpackungsform.
- Quantity: Anzahl der enthaltenen Einheiten.
- Contained Item Identifier: Kennung des enthaltenen Produkts oder der enthaltenen Einheit.
- Sponsor Package Commercial Distribution End Date: Optionales Enddatum der kommerziellen Distribution für die Verpackungsebene.
Nutzen: Verpackungsstrukturen werden nicht nur als Text beschrieben, sondern als nachvollziehbare Beziehung zwischen Verpackungskennung, enthaltenem Produkt und Menge abgebildet. Das ist besonders wichtig bei mehrstufigen Verpackungen, Sets oder großen Produktportfolios.
F-Supporting Documents – Unterstützende Dokumente
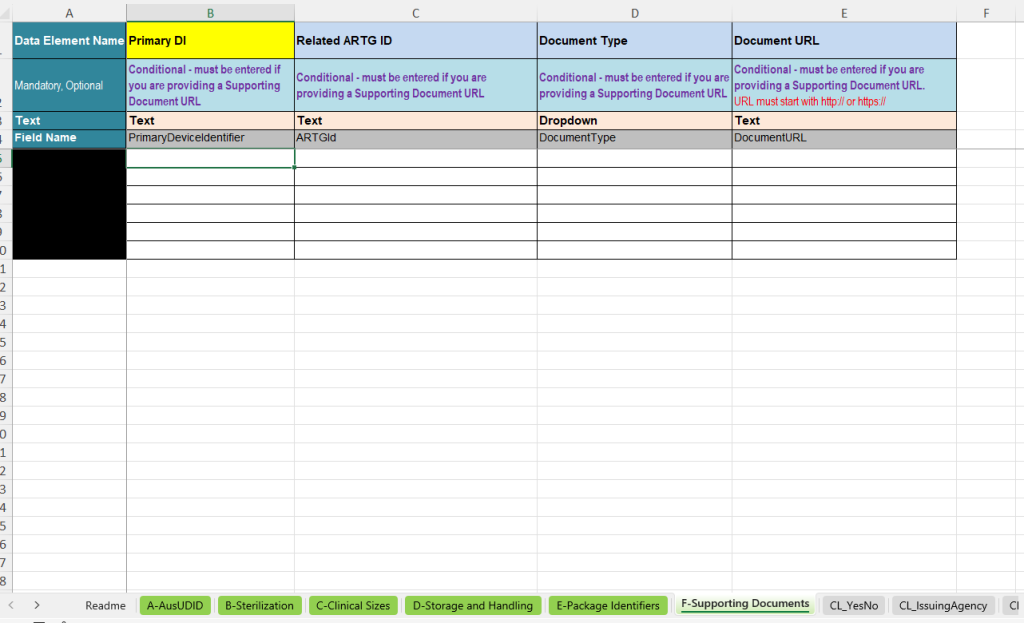
Das Register F-Supporting Documents wird verwendet, wenn produktbezogene Dokumente als URL angegeben werden sollen. Dazu gehören beispielsweise Instructions for Use oder Patient Information Leaflets.
- Primary DI: Verknüpfung mit dem entsprechenden UDI-Datensatz.
- Related ARTG ID: Bezug zur relevanten ARTG-ID.
- Document Type: Auswahl des Dokumenttyps, z. B. Instructions for Use oder Patient Information Leaflet.
- Document URL: Webadresse des Dokuments. Die URL muss mit http:// oder https:// beginnen.
Nutzen: Unterstützende Dokumente werden strukturiert mit dem UDI-Datensatz und der ARTG-Referenz verknüpft. Dadurch wird die Nachvollziehbarkeit erhöht und produktbezogene Informationen können leichter bereitgestellt werden.
Readme – Anleitung und Bearbeitungslogik
Das Register Readme enthält allgemeine Hinweise zur Verwendung der Vorlage. Es erläutert unter anderem, dass alle relevanten Excel-Blätter zu befüllen sind und dass die Register mit dem Präfix „CL_“ als Code-Listen und Eingabehilfe dienen.
- Keine neuen Spalten hinzufügen oder entfernen: Die Struktur der Vorlage darf nicht verändert werden, damit eine fehlerfreie Weiterverarbeitung möglich bleibt.
- Pflichtfelder: Rot markierte Felder müssen befüllt werden.
- Optionale Felder: Können befüllt werden, sofern die Information verfügbar oder fachlich sinnvoll ist.
- Bedingte Pflichtfelder: Müssen befüllt werden, wenn die jeweilige Bedingung erfüllt ist.
- Datumsfelder: Datumsangaben sollten als echte Excel-Datumswerte gepflegt werden.
Nutzen: Das Readme-Register reduziert Bedienfehler und stellt sicher, dass Anwender die Logik der Vorlage verstehen, bevor sie mit der Datenerfassung beginnen.
CL-Register – Code-Listen und kontrollierte Auswahlwerte
Die Register mit dem Präfix CL_ sind keine normalen Eingaberegister, sondern kontrollierte Code-Listen. Sie dienen als Grundlage für Drop-Down-Felder, standardisierte Auswahlwerte und einheitliche Terminologie innerhalb der Vorlage.
- CL_YesNo: Standardisierte Ja-/Nein- und N/A-Werte.
- CL_IssuingAgency: Unterstützte UDI-Vergabestellen wie GS1, HIBCC und ICCBBA.
- CL_Device Class: Australische Risikoklassen für Medizinprodukte und IVDs.
- CL_HandlUnitOfMeasures: Einheiten und Typen für Lagerungs- und Handhabungsbedingungen.
- CL_Sterilization: Kontrollierte Liste der Sterilisationsmethoden.
- CL_SupportingDocs: Dokumenttypen wie Patient Information Leaflet oder Instructions for Use.
- CL_DeviceIsSoftware: Auswahlwerte für Software as a Medical Device, Medizinprodukt mit Software oder „No“.
- CL_MRISafety: Werte zur MRT-Sicherheit, z. B. MR Safe, MR Conditional und MR Unsafe.
- CL_ClinicUnitOfMeasures: Umfangreiche Einheiten- und Typenliste für klinische Größenangaben.
Nutzen: Die Code-Listen reduzieren Freitext, verbessern die Datenqualität und unterstützen eine konsistente technische Weiterverarbeitung. Anwender wählen Werte aus kontrollierten Listen, anstatt Begriffe manuell und potenziell uneinheitlich einzugeben.
Bitte füllen Sie das Formular aus für ein Angebot
Intelligente Funktionen für maximale Effizienz
- Klare Registertrennung: Stammdaten, Sterilisation, klinische Größen, Lagerbedingungen, Verpackungen und Dokumente werden getrennt gepflegt.
- Primary DI als Schlüssel: Zusatzinformationen werden über den Primary Device Identifier eindeutig mit dem Hauptdatensatz verknüpft.
- Pflicht- und Bedingungslogik: Die Vorlage unterscheidet zwischen Pflichtfeldern, optionalen Feldern und bedingt erforderlichen Angaben.
- Drop-Down-gestützte Eingabe: Code-Listen unterstützen standardisierte Eingaben und reduzieren Abweichungen.
- Vorbereitung für Validierung: Die strukturierte Vorlage erleichtert die Prüfung vor technischer Aufbereitung oder Einreichung.
- Skalierbarkeit: Geeignet für einzelne Produkte ebenso wie für umfangreiche UDI-Portfolios.
Umfassendes Leistungsangebot für Ihre AusUDID-Compliance
- AusUDID UDI Excel-Vorlage: Die professionelle Basis für Ihre strukturierte UDI-Datenerfassung für Australien.
- Datenprüfung und Validierung: Wir unterstützen Sie bei der fachlichen Prüfung Ihrer UDI-Daten, damit typische Inkonsistenzen frühzeitig erkannt und korrigiert werden können.
- Technische Aufbereitung: Die strukturierten Excel-Daten können als Grundlage für technische Konvertierung, Upload-Prozesse oder M2M-Vorbereitung genutzt werden.
- AusUDID-Übertragungsservice: Wir begleiten den Prozess von der Datenerfassung über die Prüfung bis zur Vorbereitung und Unterstützung der AusUDID-Einreichung.
Technische Spezifikationen der Excel-Vorlage
- Dateiformat: Microsoft Excel (.xlsx)
- Kompatibilität: Microsoft Excel 2016 und höher
- Struktur: Ein Hauptregister, fünf fachliche Zusatzregister und mehrere Code-Listen
- Datenvalidierung: Drop-Downs und kontrollierte Wertelisten für konsistente Eingaben
- Schlüssellogik: Verknüpfung der Zusatzregister über den Primary Device Identifier
- Updates: Anpassung der Vorlage bei relevanten Änderungen der Datenanforderungen oder technischen Vorgaben
Bitte füllen Sie das Formular aus für ein Angebot
Warum führende Medizintechnikunternehmen auf unsere Lösung vertrauen
Die Europe IT Consulting GmbH ist Ihr Partner für regulatorische IT-Lösungen, UDI-Datenmanagement und technische Datenübertragungen. Wir unterstützen Unternehmen dabei, komplexe UDI-Daten strukturiert aufzubereiten und effizient für regulatorische Datenbanken nutzbar zu machen.
Das macht unsere AusUDID Excel-Vorlage einzigartig:
- Präzise Strukturierung der AusUDID-relevanten Datenelemente
- Klare Trennung zwischen Hauptdatensatz und fachlichen Zusatzinformationen
- Kontrollierte Code-Listen für standardisierte Eingaben
- Reduzierung von Validierungsfehlern durch vordefinierte Feldlogik
- Optimale Vorbereitung für manuelle Prüfung, technische Konvertierung und M2M-Prozesse
- Praxisorientierte Bedienung für Regulatory Affairs, Qualitätsmanagement, IT und externe Partner
- ANALYSIEREN: Erkennen Sie, welche AusUDID-Daten für Ihre Produkte relevant sind.
- STRUKTURIEREN: Erfassen Sie Ihre UDI-Daten in einer klaren Registerlogik.
- VALIDIEREN: Prüfen Sie Pflichtfelder, bedingte Felder und kontrollierte Auswahlwerte.
- ÜBERMITTELN: Nutzen Sie die strukturierten Daten als Grundlage für technische Aufbereitung, Upload oder M2M-Prozesse.
Perfekt abgestimmt auf Ihre individuellen Anforderungen
Für kleine und mittlere Produktportfolios:
Die Excel-Vorlage bietet eine klare Grundlage für die strukturierte Datenerfassung und spätere Prüfung.
Für große UDI-Portfolios:
Die getrennte Registerstruktur hilft, auch umfangreiche Produktdatenmengen sauber vorzubereiten und Zusatzinformationen produktbezogen zu pflegen.
Für Unternehmen mit bestehenden FDA-GUDID- oder EUDAMED-Daten:
Vorhandene UDI-Datenbestände können als Ausgangspunkt genutzt werden. Dennoch müssen die Daten für AusUDID fachlich geprüft, an die australischen Anforderungen angepasst und aktiv eingereicht werden.
Für M2M-orientierte Prozesse:
Die strukturierte Datenerfassung bildet eine wichtige Grundlage für technische Konvertierung, HL7 SPL / XML-Aufbereitung und weitere automatisierte Übertragungsprozesse.
Häufige Fragen, die Ihre Entscheidung erleichtern
Kann ich vorhandene UDI-Daten aus anderen Märkten verwenden?
Ja, vorhandene UDI-Daten aus FDA GUDID, EUDAMED oder internen UDI-Stammdaten können als Grundlage dienen. Sie müssen jedoch für die AusUDID-Anforderungen geprüft und ergänzt werden.
Kann ich mit der Excel-Vorlage selbst M2M-Dateien erzeugen?
Nein, die Excel-Vorlage dient primär der strukturierten Datenerfassung. Die technische Konvertierung in ein geeignetes Austauschformat bieten wir als separate Dienstleistung an.
Warum gibt es mehrere Register?
Nicht alle Informationen gehören in den Hauptdatensatz. Sterilisationsmethoden, klinische Größen, Lagerbedingungen, Verpackungskennungen und Dokumente können mehrfach oder bedingt auftreten. Die getrennten Register ermöglichen eine saubere und skalierbare Datenstruktur.
Welche Rolle spielt der Primary Device Identifier?
Der Primary Device Identifier ist der zentrale Schlüssel. Über ihn werden die Informationen aus den Zusatzregistern eindeutig dem richtigen Produkt zugeordnet.
Was sind die CL-Register?
CL-Register sind Code-Listen. Sie enthalten kontrollierte Werte für Drop-Down-Felder, z. B. Risikoklassen, Vergabestellen, Sterilisationsmethoden, MRI-Sicherheitsstatus oder Maßeinheiten.
Was passiert, wenn eine Spalte hinzugefügt oder gelöscht wird?
Die Struktur sollte nicht verändert werden. Zusätzliche oder entfernte Spalten können die technische Weiterverarbeitung und den Upload-Prozess beeinträchtigen.
Wer sollte die Vorlage ausfüllen?
Typischerweise arbeiten Regulatory Affairs, Qualitätsmanagement, Stammdatenmanagement, IT und gegebenenfalls der australische Sponsor zusammen. Viele Felder erfordern fachliche Abstimmung zwischen Hersteller und Sponsor.
Handeln Sie jetzt – bereiten Sie Ihre AusUDID-Daten frühzeitig vor!
Die australischen UDI-Anforderungen werden schrittweise verpflichtend. Unternehmen, die ihre UDI-Daten frühzeitig strukturieren, validieren und technisch vorbereiten, reduzieren spätere Korrekturschleifen, Upload-Risiken und operative Engpässe.
Ihr erster Schritt zu effizienter AusUDID-Compliance:
Bitte füllen Sie das Formular aus für ein Angebot
Investieren Sie jetzt in eine strukturierte regulatorische Datenstrategie für Australien.
Die AusUDID UDI Excel-Vorlage wird entwickelt und vertrieben von der Europe IT Consulting GmbH, Ihrem zertifizierten Partner für regulatorische IT-Lösungen seit 2011.
Hinweis: Bitte prüfen Sie vor Projektstart die jeweils aktuellen TGA-Vorgaben, Fristen, Rollen, Datenanforderungen und technischen Spezifikationen. Bestehende UDI-Daten aus anderen Märkten können als Ausgangsbasis dienen, ersetzen jedoch nicht die fachliche Prüfung und aktive Einreichung in AusUDID.