Die smarte Lösung für konforme UDI-Datenverwaltung in swissdamed
Strukturierte Vorbereitung Ihrer swissdamed-Produktregistrierung – effizient, nachvollziehbar und regulatorisch sauber.
Ihr Problem ist unsere Lösung
Mit swissdamed führt Swissmedic die zentrale Schweizer Datenbank für Medizinprodukte, In-vitro-Diagnostika sowie Systeme und Behandlungseinheiten. Für Hersteller, Schweizer Bevollmächtigte und weitere Wirtschaftsakteure entsteht dadurch eine neue operative Herausforderung: UDI-Daten müssen vollständig, strukturiert und entsprechend den swissdamed-Anforderungen vorbereitet, geprüft und übermittelt werden.
Unsere swissdamed Excel-Vorlage bietet Ihnen den ersten strukturierten Schritt – entwickelt von UDI-Experten für Unternehmen, die ihre Produktdaten effizient, nachvollziehbar und compliance-orientiert vorbereiten möchten.
Bitte füllen Sie das Formular aus für ein Angebot
Die swissdamed UDI Excel-Vorlage auf einen Blick:
Umfassende Register für Ihre swissdamed-relevanten UDI-Daten:
- Basic UDI-DI Registerkarte:
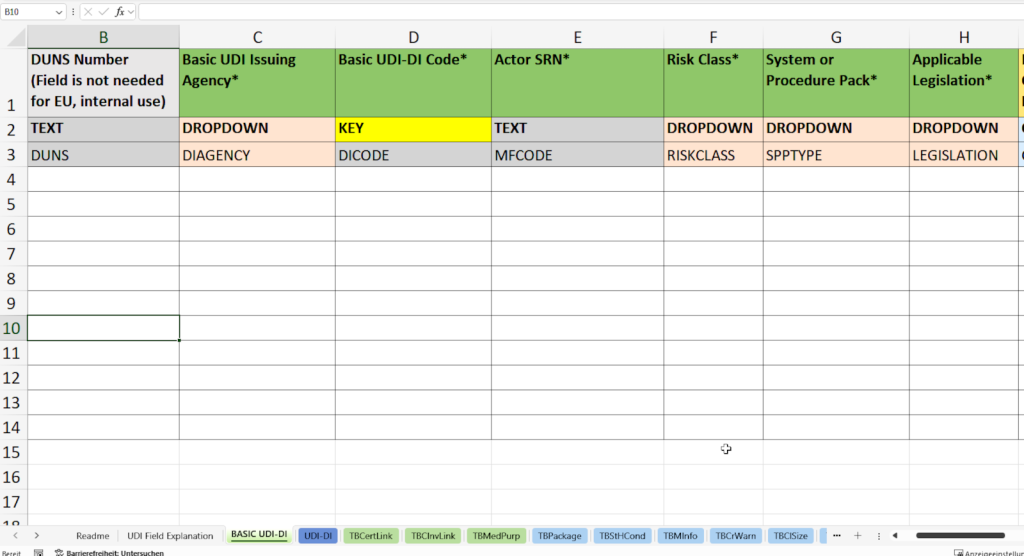 In dieser Registerkarte erfassen Sie die übergeordneten Stammdaten zur eindeutigen Identifikation Ihrer Produktfamilie. Diese Daten bilden die Grundlage für die strukturierte Zuordnung der einzelnen UDI-DIs im swissdamed UDI Devices Modul.
In dieser Registerkarte erfassen Sie die übergeordneten Stammdaten zur eindeutigen Identifikation Ihrer Produktfamilie. Diese Daten bilden die Grundlage für die strukturierte Zuordnung der einzelnen UDI-DIs im swissdamed UDI Devices Modul.
- Vergabe und Dokumentation der Basic UDI-DI nach den Spezifikationen der zuständigen Vergabestelle, z. B. GS1, HIBCC oder ICCBBA.
- Zuordnung des verantwortlichen Wirtschaftsakteurs, z. B. Schweizer Hersteller, Schweizer Bevollmächtigter oder Hersteller von Systemen und Behandlungseinheiten.
- Erfassung relevanter Akteur-Informationen, insbesondere CHRN bzw. die in swissdamed registrierten Akteurinformationen.
- Zuweisung der Produktart und Risikoklasse entsprechend den anwendbaren Anforderungen nach MedDO/IvDO bzw. den zugrunde liegenden MDR-/IVDR-Strukturen.
- Festlegung, ob es sich um ein Medizinprodukt, ein In-vitro-Diagnostikum, ein System oder eine Behandlungseinheit handelt.
- Dokumentation von Eigenschaften wie aktives Gerät, Messfunktion, Verabreichungsfunktion, implantierbares Produkt, wiederverwendbares chirurgisches Instrument oder weitere besondere Gerätetypen.
- Erfassung des Gerätemodells, Gerätenamens und weiterer beschreibender Informationen zur Produktfamilie.
- Angabe besonderer Bestandteile oder Eigenschaften, z. B. tierische oder menschliche Bestandteile, CMR-/endokrine Substanzen oder weitere regulatorisch relevante Informationen.
Bitte füllen Sie das Formular aus für ein Angebot
- UDI-DI Registerkarte:
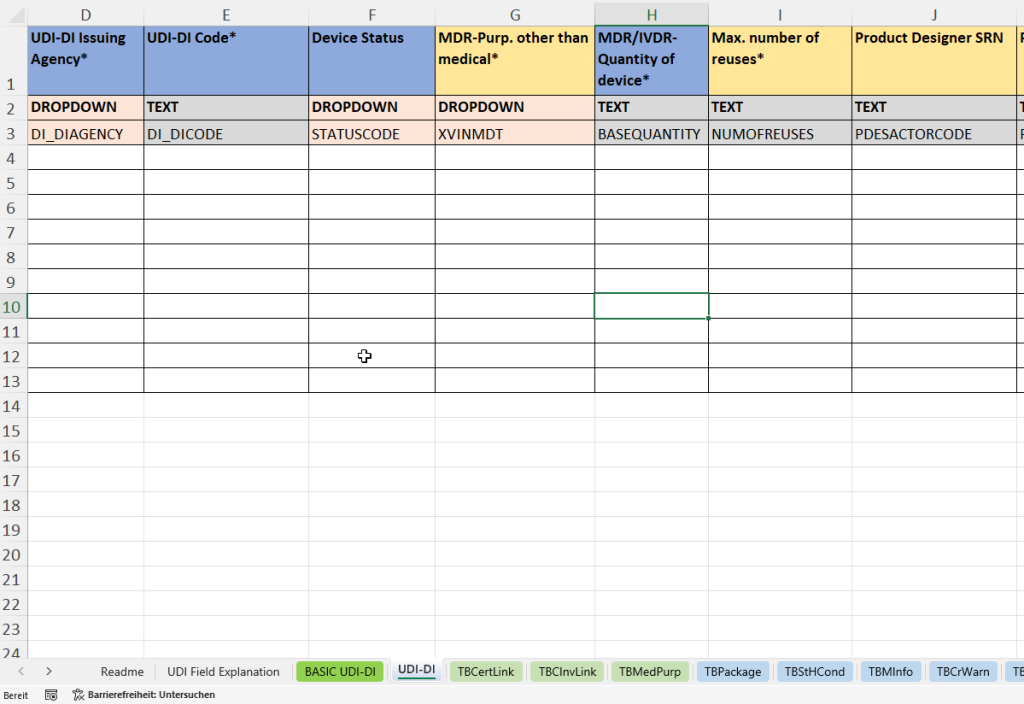 In dieser Registerkarte werden alle produktbezogenen Einzeldaten erfasst, die für die eindeutige Identifikation und Rückverfolgbarkeit eines konkreten Medizinprodukts oder IVDs erforderlich sind. Die UDI-DI dient als zentraler Identifikator für die Produktregistrierung in swissdamed.
In dieser Registerkarte werden alle produktbezogenen Einzeldaten erfasst, die für die eindeutige Identifikation und Rückverfolgbarkeit eines konkreten Medizinprodukts oder IVDs erforderlich sind. Die UDI-DI dient als zentraler Identifikator für die Produktregistrierung in swissdamed.
- Verknüpfung mit der übergeordneten Basic UDI-DI zur Einordnung in eine Produktfamilie.
- Erfassung der internen Materialnummer und Materialbeschreibung zur eindeutigen Zuordnung innerhalb Ihres Unternehmens.
- Vergabe der UDI-DI durch eine anerkannte Vergabestelle und Eintragung des eindeutigen UDI-DI-Codes.
- Festlegung des Produktstatus, z. B. aktiv, inaktiv, zurückgezogen oder in Vorbereitung.
- Erfassung der Stückzahl pro Verkaufseinheit sowie weiterer Angaben zur Produkt- und Verpackungslogik.
- Dokumentation der Referenznummer zur Identifikation in technischen Unterlagen, Etiketten oder Verpackungen.
- Angaben zur direkten Markierung am Produkt, sofern relevant.
- Sterilkennzeichnung sowie Angabe, ob eine Sterilisation vor Gebrauch erforderlich ist.
- Angabe, ob das Produkt als Einmalprodukt gekennzeichnet ist oder wiederaufbereitet wurde.
- Produktionsidentifikation: Los- oder Chargennummer, Ablaufdatum, Herstellungsdatum, Seriennummer und Softwareversion.
- Zusätzliche Identifikatoren wie sekundäre UDI-DI, Unit of Use DI oder weitere Identifikatoren, sofern erforderlich.
- Weiterführende Informationen wie URL zur elektronischen Gebrauchsanweisung oder zu zusätzlichen Produktinformationen.
- Zertifikatsinformationen:
- Erfassung des zugehörigen Basic UDI-DI-Codes zur eindeutigen Verknüpfung mit dem Zertifikat.
- Eintrag der Zertifikatsnummer und Verwaltung der Revisionsnummer, z. B. bei Verlängerungen oder Änderungen.
- Auswahl des Zertifikatstyps und Angabe der benannten Stelle, sofern für das Produkt relevant.
- Dokumentation des Ablaufdatums und weiterer Zertifikatsdaten für Produkte, bei denen diese Informationen für die Registrierung erforderlich sind.
- Klinische Prüfung / Leistungsstudie
- Eintragung relevanter Kennungen klinischer Prüfungen oder Leistungsstudien, sofern diese für das Produkt anzugeben sind.
- Angabe des Landes, in dem die klinische Prüfung oder Leistungsstudie durchgeführt wurde.
- Sprache & medizinischer Verwendungszweck
- Auswahl der Sprache, in der produktbezogene Informationen bereitgestellt werden.
- Beschreibung des medizinischen Verwendungszwecks sowie weiterer sprachabhängiger Produktinformationen.
- Verpackungsinformationen / Packaging Hierarchy:
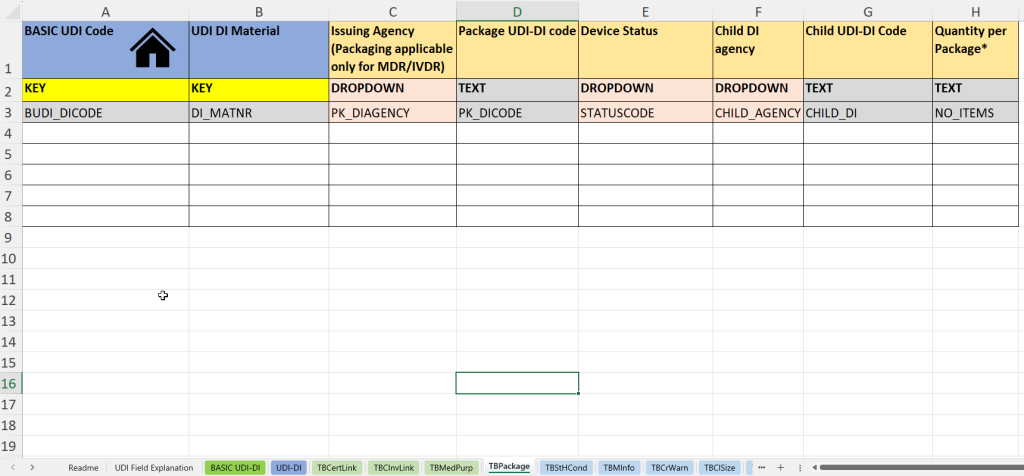 In dieser Registerkarte werden Informationen zu Verpackungseinheiten sowie zu untergeordneten UDI-DI-Strukturen dokumentiert – besonders relevant für mehrstufige Verpackungen, Sets sowie Systeme und Behandlungseinheiten.
In dieser Registerkarte werden Informationen zu Verpackungseinheiten sowie zu untergeordneten UDI-DI-Strukturen dokumentiert – besonders relevant für mehrstufige Verpackungen, Sets sowie Systeme und Behandlungseinheiten.
- Interne Materialnummer der Verpackungseinheit zur eindeutigen Identifikation.
- Vergabestelle für die Verpackungs-UDI-DI.
- Eintragung des UDI-DI-Codes der Verpackung, z. B. für Umverpackungen, Sets oder mehrstufige Verpackungshierarchien.
- Status der Verpackungseinheit.
- Angabe untergeordneter UDI-DIs innerhalb der Verpackungseinheit.
- Stückzahl pro Verpackung zur korrekten Abbildung der Verpackungshierarchie.
- Lagerungs- & Handhabungsbedingungen
- Zuordnung der Lagerungs- und Handhabungsbedingungen zur betreffenden UDI-DI.
- Angabe der Art der Bedingung, z. B. Temperatur, Feuchtigkeit, Lichtschutz oder weitere Anforderungen.
- Sprachabhängige Beschreibung zur genaueren Erläuterung besonderer Lager- oder Handhabungshinweise.
Bitte füllen Sie das Formular aus für ein Angebot
- Kritische Warnhinweise
- Auswahl und Dokumentation relevanter Warnhinweistypen, z. B. Implantat, Latex, Radioaktivität oder weitere produktbezogene Warnhinweise.
- Größenangaben
- Angabe des Größenformats, z. B. numerisch, alphanumerisch oder symbolisch.
- Genauigkeit bzw. Präzision der Größenangabe.
- Größeneinheit sowie Minimal- und Maximalwerte.
- Menschliche medizinische Substanzen
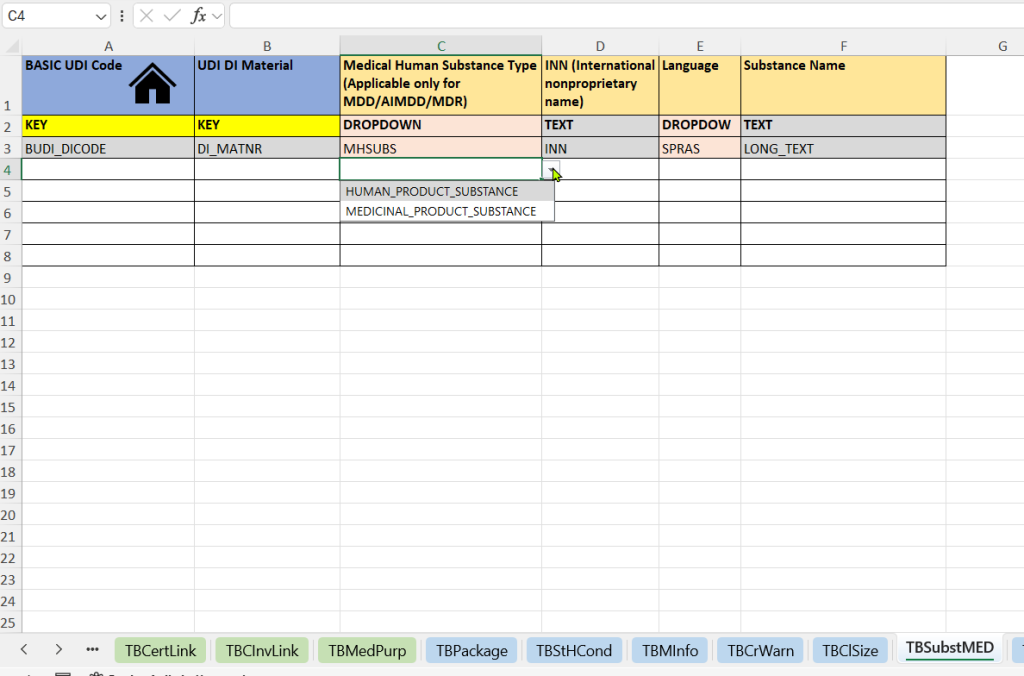
- Auswahl des Substanztyps.
- Eintragung des internationalen Freinamens, sofern vorhanden.
- Angabe der Sprache für die sprachspezifische Darstellung.
- Freitextliche Bezeichnung der Substanz, z. B. national gebräuchlicher Name oder ergänzende Beschreibung.
- CMR-/endokrine Substanzen
- Auswahl des Substanztyps, z. B. CMR-Kategorie oder endokriner Disruptor.
- Angabe des CAS-Codes und EC-Codes, sofern verfügbar.
- Sprachabhängige Bezeichnung oder Beschreibung der Substanz.
- Zusätzliche Produktbeschreibung
- Auswahl der Sprache, in der die zusätzliche Beschreibung erfolgen soll.
- Erfassung ergänzender Produktinformationen, z. B. zur Funktion, Zusammensetzung, Besonderheit des Sets oder spezifischen Produktvariante.
- Handelsname
- Auswahl der Sprache für den Handelsnamen.
- Eintragung des Handelsnamens, z. B. Produktname, Modellname oder marktrelevante Bezeichnung.
- Nomenklaturcode
- Auswahl und Dokumentation des passenden Nomenklaturcodes entsprechend den für swissdamed relevanten Vorgaben.
Bitte füllen Sie das Formular aus für ein Angebot
Intelligente Funktionen für maximale Effizienz:
- Farbliche Hervorhebung von Pflichtfeldern:

- Sofortige visuelle Identifikation obligatorischer Eingaben.
- Unterscheidung zwischen absoluten Pflichtfeldern und bedingt erforderlichen Feldern.
- Kontextbezogene Anzeige relevanter Felder auf Basis vorheriger Eingaben.
- Validierte Drop-Down-Menüs:
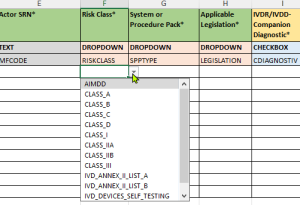
- Vordefinierte Auswahlmöglichkeiten entsprechend den swissdamed-relevanten Datenstrukturen.
- Reduzierung von Eingabefehlern durch standardisierte Optionen.
- Einheitliche Terminologie für Regulatory Affairs, Qualitätsmanagement und IT.
- Automatische Abhängigkeitsprüfungen:
- Dynamische Anpassung der Eingabefelder basierend auf Produkttyp, Klassifizierung und Akteurrolle.
- Logische Überprüfung der Datenkonsistenz zwischen verschiedenen Registerkarten.
- Warnhinweise bei potenziellen Unstimmigkeiten in der Dateneingabe.
- Zweisprachige Unterstützung:
- Parallele Beschreibungen in Deutsch und Englisch.
- Internationale Nutzbarkeit für globale Teams, Schweizer Bevollmächtigte und externe Partner.
- Konsistente Terminologie für swissdamed, UDI-Daten und regulatorische Prozesse.
- Dokumentationshilfen:
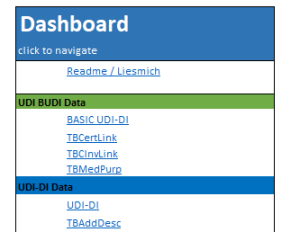
- Integrierte Erläuterungen zu komplexen Feldern.
- Hinweise zu regulatorischen Anforderungen und Datenabhängigkeiten.
- Unterstützung bei der Vorbereitung von Daten für Prüfung, Konvertierung und Übertragung.
Umfassendes Leistungsangebot für Ihre swissdamed-Compliance
- swissdamed UDI Excel-Vorlage: die professionelle Basis für Ihre strukturierte UDI-Datenerfassung und Vorbereitung der Produktregistrierung in swissdamed.
- Datenprüfung und Validierung: Wir unterstützen Sie bei der fachlichen Prüfung Ihrer UDI-Daten, damit typische Inkonsistenzen vor der Übertragung erkannt und korrigiert werden können.
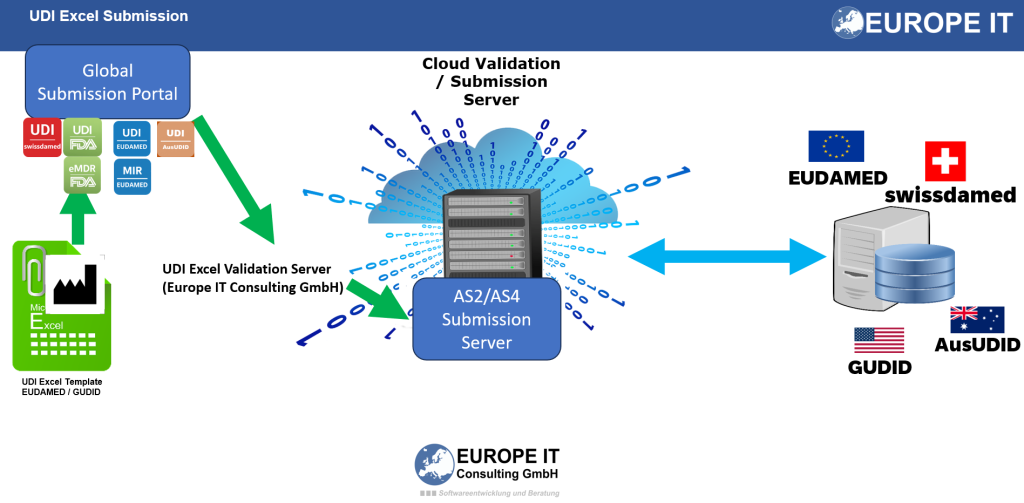
- XML- und Upload-Vorbereitung: Die Umwandlung Ihrer strukturierten Daten in ein geeignetes technisches Format erfolgt als separate Dienstleistung durch unsere Experten.
- swissdamed-Übertragungsservice: Wir begleiten den gesamten Prozess der Datenübermittlung – von der Vorbereitung über den Playground-Test bis zur produktiven Registrierung, sobald die jeweiligen Funktionen verfügbar und anwendbar sind.
Technische Spezifikationen der Excel-Vorlage
- Dateiformat: Microsoft Excel (.xlsx)
- Kompatibilität: Microsoft Excel 2016 und höher
- Größe: Optimiert für schnelle Ladezeiten, auch bei umfangreichen Datensätzen
- Sicherheit: Passwortgeschützte Strukturen zur Vermeidung unbeabsichtigter Änderungen
- Updates: Regelmäßige Aktualisierungen entsprechend neuen swissdamed-Anforderungen und technischen Spezifikationen
- Datenvalidierung: Integrierte Prüfroutinen für konsistente Eingaben
Bitte füllen Sie das Formular aus für ein Angebot
Warum führende Medizintechnikunternehmen auf unsere Lösung vertrauen
Die Europe IT Consulting GmbH ist nicht nur ISO 9001-zertifiziert und SAP-Partner – wir sind Ihr strategischer Partner für die digitale Transformation Ihrer regulatorischen Prozesse. Unser Schwerpunkt liegt auf UDI-Datenmanagement, Datenvalidierung und der technischen Vorbereitung regulatorischer Datenübertragungen.
Das macht unsere swissdamed Excel-Vorlage einzigartig:
- Präzise Strukturierung nach den Anforderungen des swissdamed UDI Devices Moduls
- Intelligente Drop-Down-Menüs mit validierten Auswahlmöglichkeiten
- Visuelle Hervorhebung von Pflichtfeldern und abhängigen Feldern
- Intuitive Navigation durch die komplexe Welt der UDI-Daten
- Mehrsprachige Unterstützung für internationale Teams, Schweizer Bevollmächtigte und externe Partner
- Optimale Vorbereitung für Datenprüfung, technische Konvertierung und swissdamed-Übertragung
- ANALYSIEREN: Erkennen Sie den Handlungsbedarf für Ihre Produktregistrierung in swissdamed. „Der erste Schritt zur strukturierten Schweizer UDI-Compliance“
- ERWERBEN: Sichern Sie sich Zugang zu unserer swissdamed Excel-Vorlage. „Der Grundstein Ihrer regulatorischen Datenstrategie für die Schweiz“
- IMPLEMENTIEREN: Erfassen Sie Ihre Produktdaten in einer klaren und prüfbaren Vorlagenstruktur. „Schluss mit unübersichtlicher UDI-Dateneingabe“
- PROFITIEREN: Beauftragen Sie uns mit Validierung, technischer Aufbereitung und swissdamed-Übertragung. „Konzentrieren Sie sich auf Ihr Kerngeschäft, während wir die technische Umsetzung begleiten“
Perfekt abgestimmt auf Ihre individuellen Anforderungen
Für kleine und mittlere Produktportfolios:
Die Excel-Vorlage ist die ideale Basis für die strukturierte Datenerfassung – ergänzt durch unseren Prüf-, Konvertierungs- und Übertragungsservice.
Für umfangreiche Produktlinien:
Die perfekte Grundlage für skalierbare Upload- oder M2M-Prozesse bei größeren Datenmengen – mit zusätzlicher Unterstützung durch unsere IT- und UDI-Experten.
Für SAP-Anwender:
Maximieren Sie Ihren Nutzen durch nahtlose Integration mit unseren UDI-Lösungen und vorhandenen regulatorischen Stammdaten.
Für Unternehmen mit bereits vorhandenen EUDAMED-Daten:
Nutzen Sie bestehende Datenbestände als Ausgangspunkt – wichtig ist jedoch: swissdamed ist eine eigenständige Schweizer Datenbank. Eine automatische Synchronisation mit EUDAMED erfolgt nicht. Die Daten müssen aktiv für swissdamed vorbereitet und eingereicht werden.
Häufige Fragen, die Ihre Entscheidung erleichtern
Fallen zusätzliche Kosten für Updates der Excel-Vorlage an?
Wichtige Updates der Vorlage sind im Erwerb enthalten, sofern sie sich auf die reguläre Pflege der Vorlagenstruktur und Wertelisten beziehen. Bei umfassenden regulatorischen oder technischen Änderungen kann eine separate Abstimmung erforderlich sein.
Kann ich mit der Excel-Vorlage selbst XML-Dateien für swissdamed erstellen?
Nein, die Excel-Vorlage dient primär der strukturierten Erfassung und Vorbereitung Ihrer UDI-Daten. Die technische Konvertierung oder Aufbereitung für den Upload bieten wir als separate Dienstleistung an.
Wie erfolgt die Übertragung meiner Daten in swissdamed?
Nach der Datenerfassung können Sie unseren Übertragungsservice in Anspruch nehmen. Je nach Projektstand und Verfügbarkeit der technischen Funktionen unterstützen wir Sie bei manueller Übertragung, XML-Aufbereitung, Playground-Tests und M2M-Vorbereitung.
Kann ich vorhandene EUDAMED-Daten für swissdamed nutzen?
Ja, vorhandene EUDAMED-Daten können häufig als wertvolle Ausgangsbasis dienen. Dennoch müssen die Daten für swissdamed geprüft, angepasst und aktiv eingereicht werden. Eine automatische Synchronisation zwischen EUDAMED und swissdamed gibt es nicht.
Welche Voraussetzungen benötige ich für swissdamed?
In der Regel muss der verantwortliche Wirtschaftsakteur in swissdamed registriert sein. Je nach Rolle betrifft dies z. B. Schweizer Hersteller, Schweizer Bevollmächtigte oder Hersteller von Systemen und Behandlungseinheiten. Für bestimmte Prozesse sind zusätzlich Benutzerrechte, Rollen und technische Zugangsdaten erforderlich.
Wie werden meine eingepflegten Daten gesichert?
Die Excel-Vorlage speichert Daten lokal in Ihrer Datei. Wir empfehlen zusätzlich regelmäßige Backups gemäß Ihren internen IT- und Qualitätsmanagementvorgaben.
Kann ich die Vorlage für mehrere Produkte oder Produktlinien verwenden?
Ja. Die Vorlage ist so konzipiert, dass mehrere Basic UDI-DIs und zahlreiche zugehörige UDI-DIs in einer strukturierten Form verwaltet werden können.
Benötige ich spezielle Excel-Kenntnisse?
Nein. Grundlegende Excel-Kenntnisse reichen aus. Die Struktur, Drop-Down-Menüs, farblichen Hinweise und Erläuterungen unterstützen die Anwender bei der Eingabe.
Wird die Vorlage bei regulatorischen Änderungen aktualisiert?
Ja. Wir beobachten die relevanten swissdamed-Entwicklungen und passen die Vorlage an, wenn sich Datenstrukturen, Wertelisten oder technische Anforderungen ändern.
Handeln Sie jetzt – sichern Sie sich Ihren Vorsprung für die Schweizer Produktregistrierung!
Die swissdamed-Registrierungspflichten rücken näher. Unternehmen, die ihre UDI-Daten frühzeitig strukturieren, validieren und technisch vorbereiten, reduzieren spätere Risiken, Korrekturschleifen und operative Engpässe.
Ihr erster Schritt zu effizienter swissdamed-Compliance:
Bitte füllen Sie das Formular aus für ein Angebot
Investieren Sie jetzt in eine strukturierte regulatorische Datenstrategie für die Schweiz.
Die swissdamed UDI Excel-Vorlage wird entwickelt und vertrieben von der Europe IT Consulting GmbH, Ihrem zertifizierten Partner für regulatorische IT-Lösungen seit 2011.