Neue MDCG-Leitlinie zur Master UDI-DI für Brillenfassungen, Brillengläser und Fertiglesebrillen veröffentlicht
Mit dem Dokument MDCG 2025-8 Rev. 1 hat die Medical Device Coordination Group im März 2026 eine neue Leitlinie zur praktischen Umsetzung der Master UDI-DI für spectacle frames, spectacle lenses und ready-to-wear reading spectacles veröffentlicht. Das Dokument erläutert, wie Hersteller diese hochgradig individualisierten Produkte künftig im UDI-System strukturieren, kennzeichnen und in EUDAMED registrieren sollen.
Die Leitlinie steht im Zusammenhang mit der Delegierten Verordnung (EU) 2025/1920, durch die für diese Produktgruppen spezielle Regeln zur UDI-Zuweisung eingeführt wurden. Dabei ist die Master UDI-DI als Identifier für Gruppen hoch individualisierter Produkte gedacht und übernimmt für diese Konstellationen die Rolle der UDI-DI im Sinne der MDR. Das Dokument behandelt insbesondere die Struktur der Identifier, die Zuweisungslogik, die Kennzeichnung, die Verpackungsebenen, die Vigilance-Berichterstattung und die EUDAMED-Registrierung.
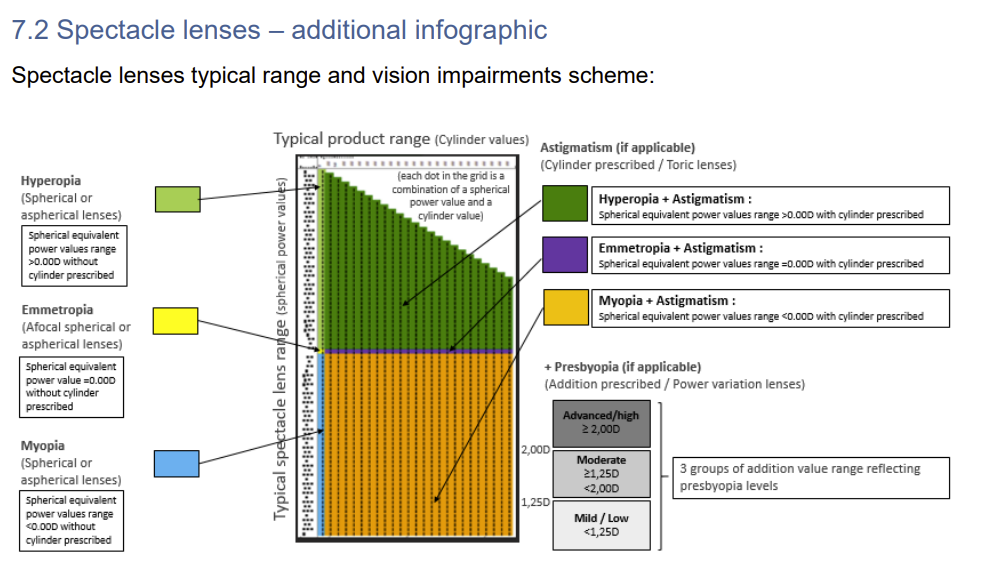
Besonders relevant ist die jetzt veröffentlichte Revision 1, auch wenn sie inhaltlich nur punktuelle Anpassungen enthält. Die MDCG nennt ausdrücklich zwei Änderungen im Bereich der Brillengläser: Zum einen wurde in einer Grafik die Bezeichnung von „Advanced“ auf „Advanced/High“ korrigiert. Zum anderen wurde im Entscheidungsbaum für die Master-UDI-DI-Zuweisung der Schwellenwert für diese Kategorie fachlich richtiggestellt: Statt „< 1,25 D“ gilt für Advanced/High nun „≥ 2.00 D“. Damit wird die Einordnung der Additionswerte für Presbyopie klarer und konsistenter dargestellt.
Inhaltlich macht die Leitlinie deutlich, dass sich die Logik der Master UDI-DI von der klassischen UDI-DI-Zuweisung unterscheidet. Während die Basic UDI-DI die Gruppe von Produkten mit gleichem Verwendungszweck, gleicher Risikoklasse und gleichen wesentlichen Designmerkmalen beschreibt, dient die Master UDI-DI dazu, hoch individualisierte Produkte anhand definierter Designparameter weiter zu gruppieren. Für die betroffenen Produktgruppen gilt außerdem: Master UDI-DI und UDI-PI bilden zusammen die UDI, die Master UDI-DI erscheint auf dem Label und wird auch in EUDAMED verwendet.
Für Brillenfassungen beschreibt die Leitlinie eine Zuweisungslogik, die sich zunächst auf die Basic UDI-DI stützt. Diese basiert auf den Parametern Rahmenkonstruktion und Rahmenmaterial. Die Master UDI-DI wird anschließend zusätzlich über die horizontale Kastenscheibenbreite gebildet, typischerweise im Bereich von 40 mm bis 60 mm. Markenname oder Modellreferenz sind dabei ausdrücklich keine Master-UDI-DI-Trigger.
Für Brillengläser ist die Logik deutlich komplexer. Die Basic UDI-DI basiert hier auf Commercial Indexes bzw. Materialtypen sowie auf dem Glasdesign. Die Master UDI-DI wird dann anhand von Gruppen des sphärischen Äquivalents, von Additionswerten und von ähnlichen Sehbeeinträchtigungen bestimmt. Die Leitlinie erklärt hierzu auch die Berechnung des sphärischen Äquivalents und ordnet Produkte anhand dieser Werte etwa Gruppen wie Myopie, Hyperopie, Astigmatismus oder Presbyopie zu. Gerade in diesem Bereich ist die jetzt korrigierte Abgrenzung der Kategorie Advanced/High praktisch relevant.
Für Fertiglesebrillen wird die Basic UDI-DI aus den Parametern Rahmenkonstruktion, Rahmenmaterial und Linsenmaterial abgeleitet. Die Master UDI-DI ergänzt dies um zwei weitere Designparameter: die horizontale Kastenscheibenbreite sowie die sphärische Linsenstärke, die in der Leitlinie für den Bereich +1.00 D bis +3.50 D beschrieben wird. Auch hier dienen Marken und Katalognummern nicht als eigentliche Zuweisungskriterien für die Master UDI-DI.
Ebenfalls wichtig sind die Aussagen zu Packaging und Vigilance. Höhere Verpackungsebenen können grundsätzlich eine eigene Master UDI-DI benötigen, sofern sie den Inhalt regulatorisch abbilden müssen. Typische Versandkartons mit gemischten Inhalten werden jedoch meist als logistische Versandcontainer betrachtet und sollen in der Regel keine eigene Master UDI-DI erhalten, die ihren Inhalt widerspiegelt. Im Vigilance-Fall verlangt die Leitlinie, dass Hersteller die UDI aus Master UDI-DI und UDI-PI angeben und betroffene Produkte zusätzlich über interne Rückverfolgbarkeitssysteme präzise eingrenzen können.
Auch der Zeitplan wird noch einmal klar benannt: Die Delegierte Verordnung wurde am 23.09.2025 im Amtsblatt veröffentlicht, trat am 13.10.2025 in Kraft und ist ab dem 01.11.2028 anzuwenden. Produkte, die vor dem 1. November 2028 hergestellt wurden, müssen laut Leitlinie noch keine Master UDI-DI auf dem Label tragen. Für Hersteller bedeutet das: Die operative Vorbereitung sollte frühzeitig beginnen, auch wenn die verbindliche Anwendung erst später greift.
Fazit:
Mit MDCG 2025-8 Rev. 1 liegt nun eine konkrete Orientierungshilfe für die Umsetzung der Master UDI-DI bei Brillenfassungen, Brillengläsern und Fertiglesebrillen vor. Die Revision selbst bringt keine neue Frist und keine grundlegende Systemänderung, präzisiert aber einen fachlich wichtigen Punkt bei der Klassifizierung von Additionswerten für Brillengläser. Für Hersteller ist das Dokument vor allem deshalb relevant, weil es die praktische Logik der Gruppierung, Kennzeichnung und späteren EUDAMED-Registrierung deutlich greifbarer macht.
Bitte lesen Sie hierzu auch unsere News zum Zeitplan zur Einführung der Master UDI-DI.









Related Posts