EUDAMED Status
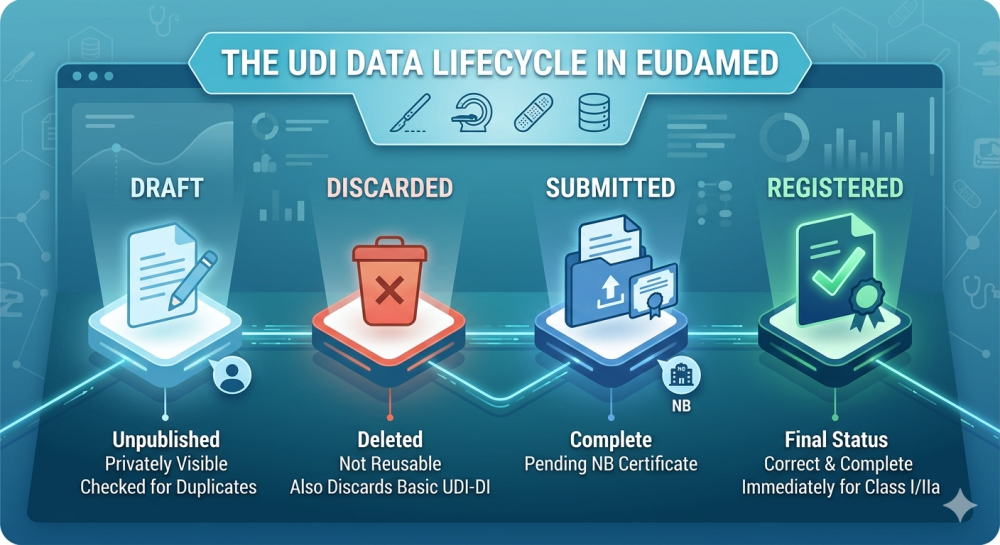
EUDAMED Status Was bedeuten Draft, Discarded, Submitted und Registered bei UDI-Daten? Wer UDI-Daten in EUDAMED pflegt oder über XML bzw. M2M überträgt, stösst regelmässig auf unterschiedliche Datensätze-Status. In der Praxis…

EUDAMED Status Was bedeuten Draft, Discarded, Submitted und Registered bei UDI-Daten? Wer UDI-Daten in EUDAMED pflegt oder über XML bzw. M2M überträgt, stösst regelmässig auf unterschiedliche Datensätze-Status. In der Praxis…
2026 erhöht den Handlungsdruck für Hersteller 2026 ist für viele MedTech-Unternehmen operativ anspruchsvoll. In der EU werden ab 28. Mai 2026 die ersten vier EUDAMED-Module verpflichtend, nämlich Actor Registration, UDI/Device…
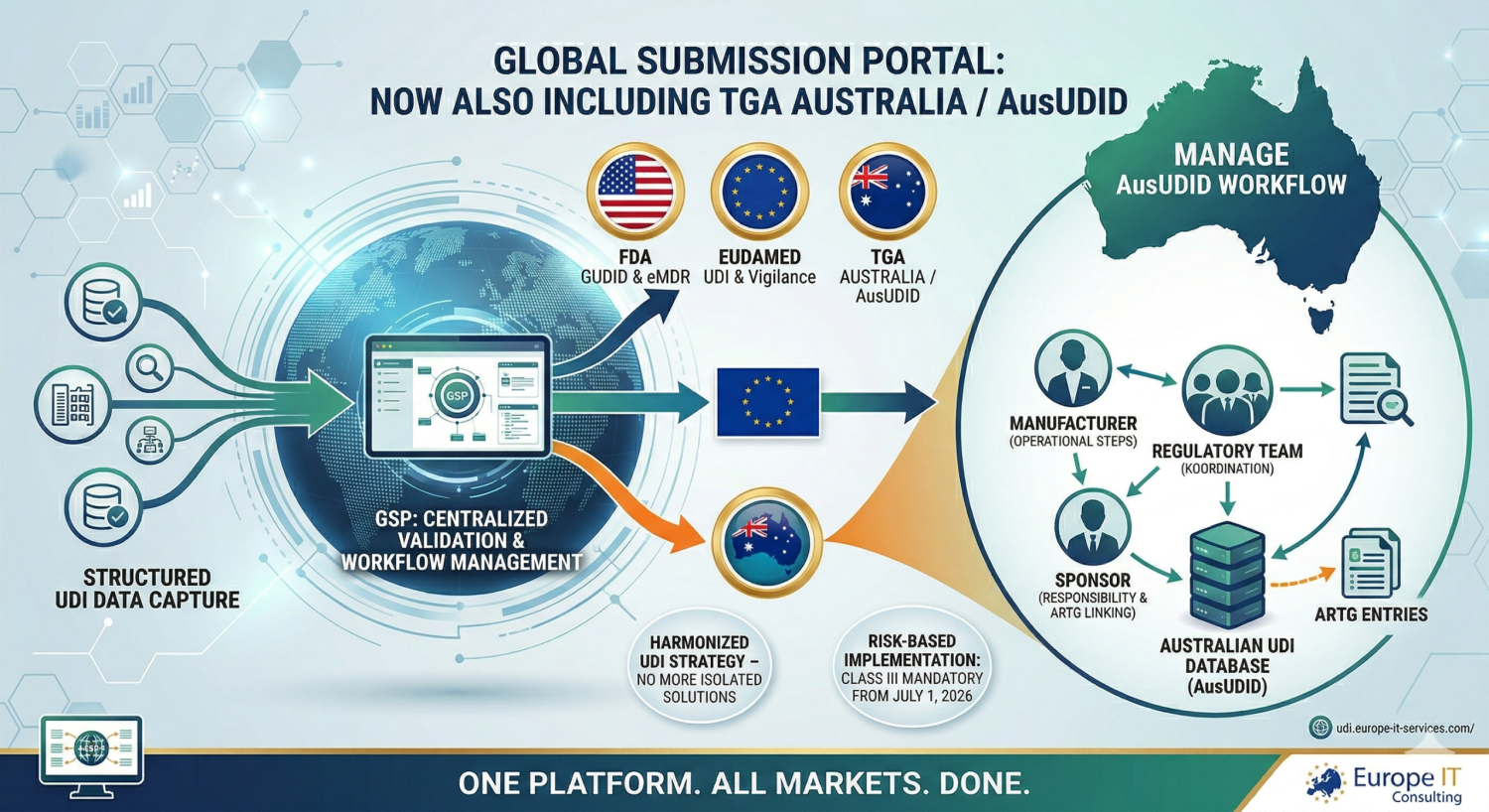
Australien im GSP: UDI-Daten strukturiert erfassen, validieren und zentral für den AusUDID-Workflow steuern Das Global Submission Portal wächst weiter: nach dem Launch mit FDA eMDR, FDA GUDID und EUDAMED UDI…
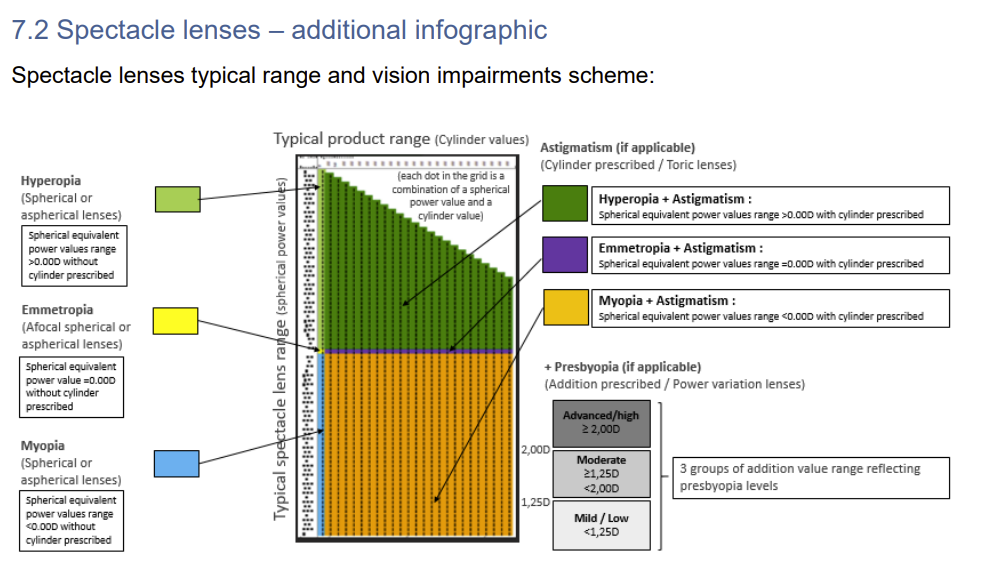
Neue MDCG-Leitlinie zur Master UDI-DI für Brillenfassungen, Brillengläser und Fertiglesebrillen veröffentlicht Mit dem Dokument MDCG 2025-8 Rev. 1 hat die Medical Device Coordination Group im März 2026 eine neue Leitlinie…

regularia 2026: persönliche Gespräche, starke Marktimpulse und wertvolle Einblicke für die digitale Regulatory-Praxis Die regularia 2026 hat einmal mehr gezeigt, wie stark sich die Medizintechnikbranche im Spannungsfeld zwischen regulatorischen Anforderungen,…
EUDAMED-Datenmanagement: Europe IT Consulting GmbH deckt kritische Fehlerquellen bei UDI-Updates auf Die Experten der Europe IT Consulting GmbH haben eine signifikante Schwachstelle in der EUDAMED-Architektur identifiziert, die die Datenpflege für…
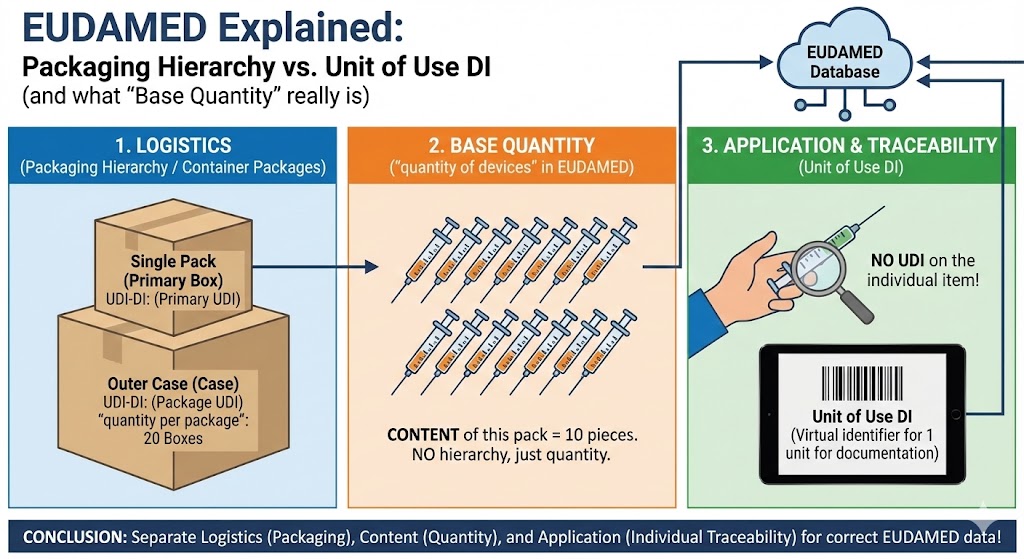
EUDAMED verständlich erklärt: Verpackungshierarchie vs. Unit of Use DI (und was „Base Quantity“ wirklich ist) In EUDAMED werden drei Themen besonders häufig verwechselt: Verpackungshierarchie (Container Packages), Unit of Use DI…

swissdamed Updates: EMDN-Codes und Legacy Devices Swissmedic hat zwei zentrale swissdamed-Releases veröffentlicht: Mit Version 2.2.1 wird das aktuelle EUDAMED-Schema (XSD 3.0.25 / Plattform 2.22.0) unterstützt – inklusive aktualisierter EMDN-Codes. Kurz…

EUDAMED UDI-Registrierung meistern – Wo anfangen & wie Unsicherheiten überwinden? Die Registrierung von Medizinprodukten in der europäischen Datenbank EUDAMED wirkt für viele Hersteller wie ein Mammutprojekt: neue Rollen, neue Datenlogik…

Global Submission Portal: Jetzt auch MIR Reporting (EUDAMED Vigilance) Endlich: EU Manufacturer Incident Reports zentral erfassen, validieren und einreichen – in einem Workflow. Das Global Submission Portal erreicht die nächste…