Australien im GSP:
UDI-Daten strukturiert erfassen, validieren und zentral für den AusUDID-Workflow steuern
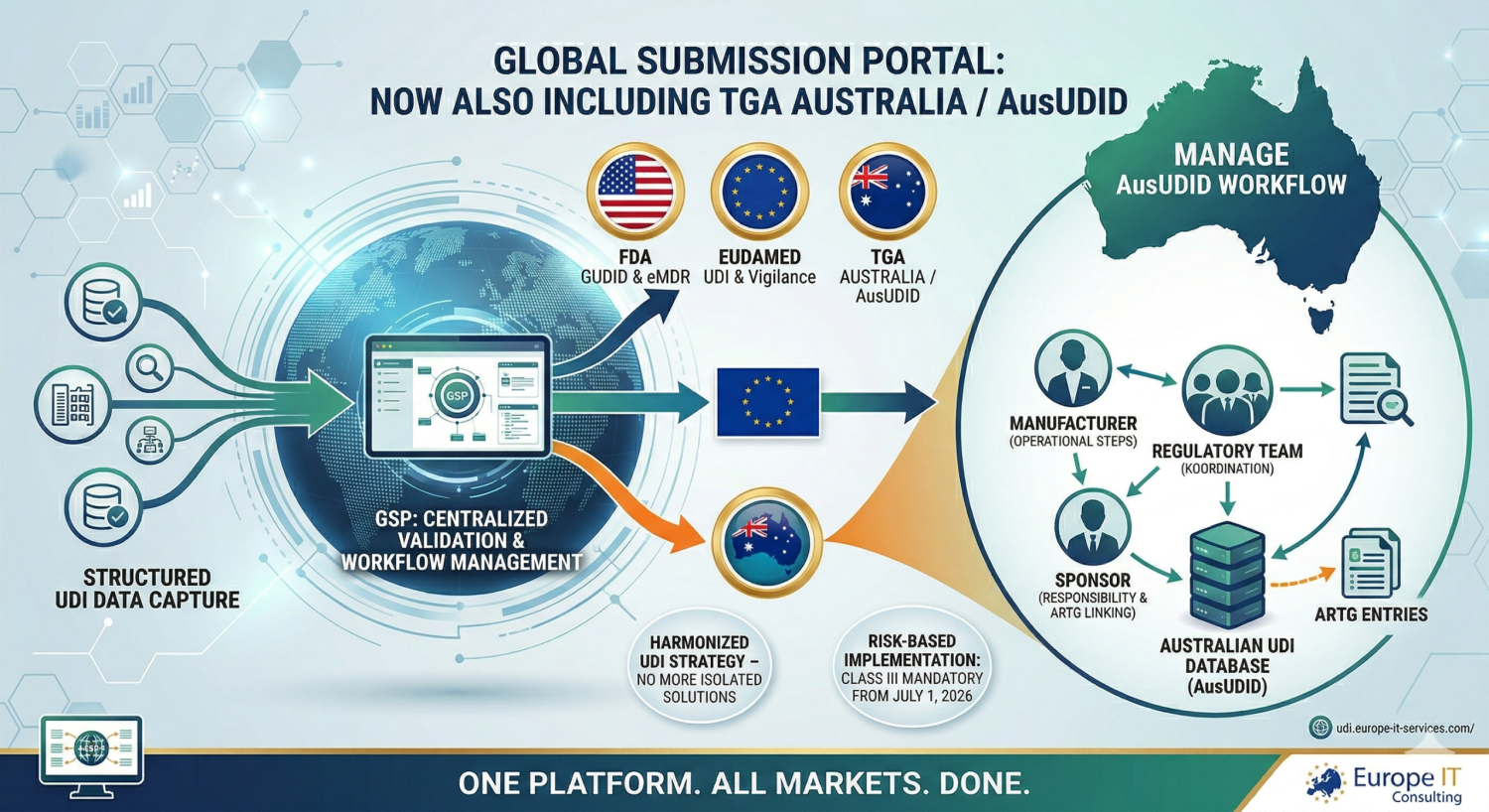
Das Global Submission Portal wächst weiter: nach dem Launch mit FDA eMDR, FDA GUDID und EUDAMED UDI sowie der Erweiterung um EUDAMED Vigilance unterstützen wir nun auch Australien. Damit wird das GSP zu einer noch stärkeren zentralen Plattform für globale Regulatory-Submission-Prozesse.
Dieser Zeitpunkt ist bewusst gewählt. Australien hat sein UDI-System regulatorisch bereits 2025 eingeführt, die Australian UDI Database (AusUDID) ist live, und die Umsetzung erfolgt risikobasiert über mehrere Jahre. Für Hersteller und Sponsoren von Class III sowie Class IIb Medical Devices wird UDI ab dem 1. Juli 2026 verpflichtend, weitere Klassen folgen in den darauffolgenden Jahren.
AusUDID: Zentrale Datenbasis für den australischen Markt
Mit der AusUDID schafft die TGA eine zentrale Datenbasis für UDI-DIs und die dazugehörigen Gerätedaten in Australien. Die veröffentlichten UDI-Datensätze werden mit den relevanten ARTG-Einträgen verknüpft.
Genau hier setzt das Global Submission Portal an: Es hilft dabei, UDI-relevante Daten strukturiert vorzubereiten, Prüf- und Freigabeprozesse besser zu organisieren und Submission-Workflows in eine einheitliche Umgebung zu überführen.
Australien als Teil der globalen UDI-Strategie
Besonders wichtig für international aufgestellte MedTech-Unternehmen: Australien ist kein isolierter Sonderfall mehr, sondern ein weiterer Markt, der in die globale UDI-Strategie integriert werden muss. Wer bereits FDA- oder EUDAMED-Prozesse steuert, profitiert von einem harmonisierten Vorgehen statt von zusätzlichen Insellösungen.
Genau diese Vereinheitlichung ist der Ansatz des GSP:
- weniger Medienbrüche
- mehr Transparenz
- klarere Statusführung
- und eine bessere operative Beherrschbarkeit der regulatorischen Einreichungen
Rollenlogik in Australien: Sponsor, Hersteller, Regulatory Team
Regulatorisch ist die Rollenlogik in Australien wichtig: Sponsoren bleiben für die Einreichung und Pflege der UDI-Records verantwortlich. Hersteller können im AusUDID zwar viele operative Schritte übernehmen, die Verknüpfung mit dem ARTG bleibt jedoch sponsorenseitig relevant. Für Unternehmen mit internationalen Strukturen ist deshalb nicht nur die Datenerfassung entscheidend, sondern auch ein sauber gesteuerter Workflow zwischen Hersteller, Sponsor und Regulatory Team.
Eine Plattform. Alle Märkte. Fertig.
Mit der Erweiterung um TGA Australia / AusUDID baut Europe IT Consulting das Global Submission Portal konsequent weiter aus. Ziel bleibt unverändert: globale Submission-Prozesse für MedTech-Unternehmen übersichtlicher, robuster und effizienter zu machen – in einem System.
Stellen Sie Ihre Anfrage direkt hier: https://udi.europe-it-services.com/








Related Posts