MDCG veröffentlicht Zeitplan zur Einführung der Master UDI-DI für Sehhilfen und Kontaktlinsen
Die Medical Device Coordination Group (MDCG) hat mit dem Positionspapier MDCG 2025-7 die verbindlichen Zeitpläne für die Einführung der Master UDI-DI bei stark individualisierten Medizinprodukten veröffentlicht. Betroffen sind:
-
Kontaktlinsen
-
Brillenfassungen
-
Brillengläser
-
Fertiglesebrillen
Hintergrund
Die Master UDI-DI ist ein neues Identifikationskonzept für hoch individualisierte Produkte. Es ermöglicht, ähnliche Produkte mit identischen Designmerkmalen unter einer gemeinsamen Kennung in EUDAMED zu registrieren. Ziel ist, die Zahl der UDI-Datensätze zu reduzieren und die Verwaltung für Hersteller, Händler und Behörden zu vereinfachen.
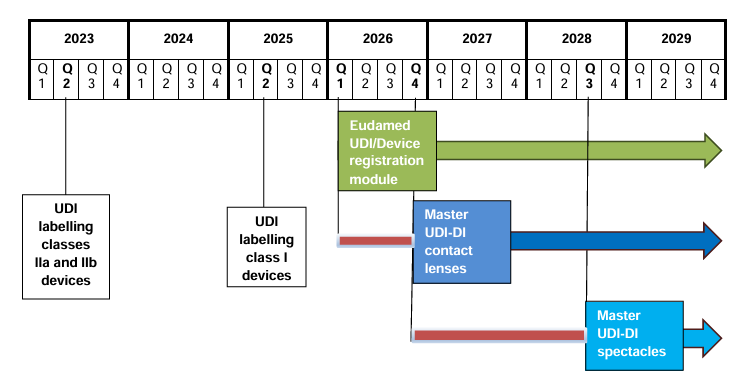
Wichtige Fristen im Überblick
| Produktkategorie | UDI-Label-Pflicht | Pflicht zur Nutzung des EUDAMED-UDI-Registrierungsmoduls | Pflicht zur Master UDI-DI | Übergangsphase |
|---|---|---|---|---|
| Kontaktlinsen | 26. Mai 2023 (Klasse IIa/IIb) | Q1 2026 | 9. November 2026 | Q1 2026 – Q4 2026 |
| Brillenfassungen, Brillengläser, Fertiglesebrillen | 26. Mai 2025 (Klasse I) | Q1 2026 | September 2028 | Q1 2026 – Q3 2028 |
Freiwillige Umsetzung empfohlen
Hersteller können die Master UDI-DI bereits vor den Pflichtterminen vergeben. Die MDCG empfiehlt, diese Möglichkeit zu nutzen, um:
-
frühzeitig Erfahrung mit der neuen Kennung zu sammeln
-
Vigilanzmeldungen und Post-Market Surveillance effizienter zu gestalten
-
interne Prozesse rechtzeitig anzupassen
Bedeutung für die Branche
Mit der Einführung der Master UDI-DI wird ein wichtiger Schritt zur Harmonisierung und Entlastung bei der UDI-Verwaltung umgesetzt. Für Hersteller bedeutet dies allerdings, dass technische und organisatorische Vorbereitungen bereits jetzt starten sollten.
Weiterführende Informationen:








Related Posts